Svag i knäna: Miller Fisher syndrom
Miller Fisher syndrom (MFS), en sällsynt, självbegränsande variant av Guillain-Barr Xia syndrom (GBS), är ett anti-GQ1bIgG-antikroppssyndrom som påverkar perifera och centrala nervsystemet.1 ett akut neuromuskulärt polyneuropatiskt tillstånd, MFS orsakar en stigande förlamning med en klassisk presentationstriad av oftalmoplegi, ataxi och areflexi. Forskare beskrev först den kliniska triaden 1932.1 två decennier senare var den kanadensiska strokespecialisten Charles Miller Fisher den första som publicerade en rapport 1956 som beskrev de kliniska fynden och definierade tillståndet som en begränsad form av GBS.2
symtom uppträder under flera dagar, ofta på vintern och våren, vanligtvis efter en virusinfektion, och patienter upplever ofta diplopi som ett av de första symptomen. När en patient uppvisar symtom som intermittent esotropi, försämrade horisontella sysslor och fasta mydriatiska elever, och din neurologiska undersökning är onormal, är det dags att tänka på GBS, särskilt MFS. Följande fall illustrerar relevanta tecken och symtom och återspeglar det typiska resultatet.
historia
en 27-årig kaukasisk man presenterades för VA Eye Clinic under vårmånaderna och rapporterade akut debut binokulär diplopi som startade en dag tidigare. Patienten uppgav att det var konstant men inträffade endast vid distansvisning med föremål förskjutna horisontellt. Det fanns ingen ögonsmärta eller suddig syn i samband med diplopi. Han klagade också på nyligen yrsel och balanssvårigheter. Han rapporterade en sinusinfektion med signifikant paranasal trängsel som började en vecka före dubbelsyn. Tidigare okulära och medicinska historier var unremarkable; patienten tog för närvarande inga mediciner och hade inga läkemedelsallergier.
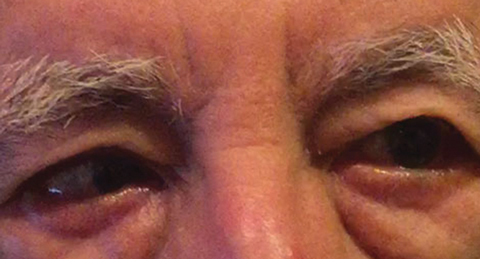
Fig. 1. Differentialdiagnosen efter baslinjeundersökningen inkluderade en partiell rätt cn VI pares, vilket kan indikera ett vaskulärt tillstånd, vilket ses här hos en annan patient. Klicka på bilden för att förstora. Foto: Michael DelGiodice, od
diagnostiska Data
vid baslinjeundersökning var okorrigerade visuella acuiteter 20/20-2 OD och 20/25-2 OS. Eleverna var 5 mm lika runda och reaktiva mot ljus utan afferent pupilldefekt. Extraokulära motilities var fulla, släta och exakta i båda ögonen utan begränsningar. Täcktest på avstånd avslöjade en intermittent fyra till sex prisma diopter rätt esotropia i primär blick som inträffade ungefär 50% av tiden. Utför täcktest på nära avslöjade en fyra prisma diopter esophoria i primär blick utan tropia.
även om det inte genomförs i detta fall bör kliniker täcka test i primär, höger och vänster blick. Hos patienter med diplopi kommer kranial nerv sex (CN VI) pares att manifesteras som icke – komitant avvikelse, värre i höger eller vänster blick, beroende på vilken sida paresen är på. En dekompenserande phoria kommer å andra sidan att visa comitant avvikelse.
brytningsfel var -0.50 d sphere OD och -0.75 d sphere OS och vision var korrigerbar till 20/20 i varje öga. Intraokulära tryck var inom normala gränser i båda ögonen. Främre och bakre segmentfynd var obemärkliga i höger och vänster ögon. De optiska nerverna verkade friska med ett förhållande mellan kopp och skiva på 0,15 i båda ögonen.
differentiella diagnoser inkluderade en partiell höger cn VI pares (Figur 1), myasthenia gravis, en komprimerande process och ett dekompenserande avstånd esophoria orsakar en intermittent höger esotropi. Patienten förnekade någon tidigare historia av binokulär diplopi.
avbildning av hjärnan och banorna beställdes av ögonkliniken för att utesluta hjärnans engagemang, inklusive en komprimerande lesion. Datortomografi (CT) skanningar av hjärnan och banorna utfördes och tolkades av personalneuroradiologen. CT valdes istället för magnetisk resonansavbildning (MRI) på grund av tidpunkt och tillgänglighet; testning och resultat kunde erhållas samma dag med CT i kliniken efter timmar. Resultaten var obemärkliga utan tecken på intrakraniell blödning, kompressionsskada eller akut infarkt.
CT i paranasala bihålor avslöjade måttlig till svår kronisk paranasal sinus sjukdom och fullständig opacifiering av höger maxillary sinus. Det fanns ingen förlängning i banan. Patientens husläkare informerades om patientens symtom, ögonundersökningsresultat och CT-avbildningsresultat och inledde behandling för maxillary bihåleinflammation med ett oralt azitromycin fem dagars dospaket och instruerade patienten att följa upp med ögonkliniken.
patienten återvände fem dagar senare efter att ha avslutat sin orala azitromycinkurs och uppgav att han inte upplevde någon förbättring av distansdiplopi; dessutom upplevde han uppkomsten av signifikant fotofobi och periokulär smärta runt båda ögonen. Patienten uppgav att hans gångobalans och gångproblem också försämrades. Vid undersökning förblev bäst korrigerade visuella acuiteter 20/20 i höger och vänster ögon. Eleverna utvidgades vid 8,5 mm utan reaktivitet mot ljus i båda ögonen (Figur 2). Extraokulära motiliteter avslöjade lateral begränsning med smärta vid rörelse i höger öga och medial begränsning med smärta vid rörelse i vänster öga i överensstämmelse med en höger blick pares (Figur 3). Horisontella och vertikala sysslor var saccadic med felaktiga och ryckiga rörelser. Främre och bakre segmentfynd förblev unremarkable OU.
differentiella diagnoser efter oftalmologisk undersökning inkluderade vänster internukleär oftalmoplegi, höger blick pares och höger blick pares med vänster internukleär oftalmoplegi, vilket kan redogöra för extraokulära motilitetsfynd. Andra skillnader inkluderar en mellanhjärnskada eller myasthenia gravis. Differentiella diagnoser för pupillutvidgning inkluderar tredje nerv (CN III) pares, trauma och farmakologisk utvidgning. Patienten hade inga andra fynd som överensstämde med en tredje nervpares och nekade trauma eller exponering för farmakologiska medel.
patienten hänvisades till neurologi för vidare bedömning. Neurologisk undersökning rapporterade att patienten var helt vaken och orienterad utan förlust av ansiktssensation. Patienten uppvisade mild ataxi med svårigheter att gå i tandem och stå från en hukande position. Proximal svaghet i både övre och nedre extremiteter och onormala reflexer var närvarande. Alla sensoriska modaliteter var intakta. MR och magnetisk resonansangiografi (mra) i hjärnan och banorna var obemärkliga. Cerebrospinalvätskeprotein höjdes vid 75 mg/dL (referensområde: 15 mg/dL till 45 mg / dL) utan andra avvikelser. Elektromyogramtestning var unremarkable och visade inga abnormiteter i nervledning från ryggraden till fötter och händer.
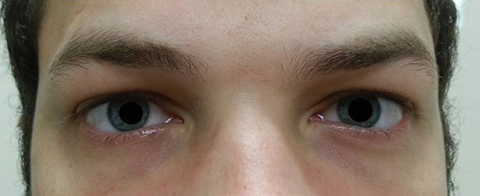
Fig. 2. Patientens elever utvidgades 8,5 mm utan reaktivitet i höger eller vänster ögon. Klicka på bilden för att förstora.
diagnos
patienten presenterade akuta symtom på diplopi, ataxi och areflexi. Med tanke på intermittent höger esotropi, försämrade horisontella sysslor, fast mydriatisk elev, mild ataxi och onormala reflexer vid neurologisk undersökning och förhöjt cerebrospinalvätskeprotein, diagnostiserades MFS. Patienten togs in på sjukhuset för att övervaka eventuella ytterligare komplikationer. En ögonplåster tillhandahölls patienten för att täcka det högra ögat efter behov för diplopi.
inga publicerade diagnostiska kriterier för Miller Fisher syndrom finns för närvarande. Diagnosen ställs vanligtvis genom presentationen av den kliniska triaden tillsammans med avbildning och cerebrospinalvätskestudier. MR är vanligtvis unremarkable i tillståndet, även om vissa studier har visat centrala lesioner i mellanhjärnan, pons och nedre medulla. Elektrofysiologiska studier visar minskad eller onormal perifer sensorisk ledning.17
Cerebrospinalvätskeprotein är ofta förhöjt utan andra onormala fynd. I en landmärkestudie visade 64,4% av MFS-patienterna förhöjt spinalvätskeprotein.8 ett positivt Anti-GQ1b IGG-antikroppstest möjliggör en definitiv diagnos. I en studie var anti-GQ1b IgG-antikropp närvarande hos upp till 95% av patienterna med tillståndet och frånvarande i kontroller.3
neurologen diagnostiserade patienten med MFS baserat på den kliniska triaden av oftalmoplegi, ataxi och areflexi, en obekväm MR och MRA i hjärnan och förhöjt cerebrospinalvätskeprotein. Därför utfördes inte Anti-GQ1b IGG-antikroppstestning i detta fall.
flera kliniska egenskaper hos MFS ses också i Guillain-Barr Bisexuell syndrom och Bickerstaffs hjärnstammencefalit, vilket gör diagnosen utmanande. Patienter med endast Guillain-Barr Bisexuell närvarande med lem svaghet, sensorisk förlust, kranial neuropati och areflexi utan oftalmologiska manifestationer. Patienter med bickerstaffs hjärnstammencefalit förekommer vanligtvis med oftalmoplegi, ataxi, hyperreflexi och ett stört medvetande. Eftersom flera symtom och tecken finns i alla tre tillstånd, är anti-GQ1b IGG-antikroppstitertestning till hjälp för en mer definitiv diagnos. Anti-GQ1b IgG-antikropp är positiv hos en stor majoritet av Miller Fisher syndrompatienter jämfört med 66% hos Bickerstaffs hjärnstamsencefalit och 26% av Guillain-Barr-patienter.16
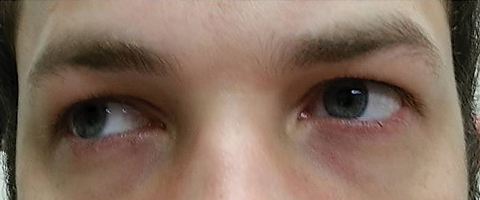
Fig. 3. Extraokulära motiliteter avslöjade begränsning i dextroversion. Klicka på bilden för att förstora.
behandling och uppföljning
patienten utvärderades dagen efter antagning, då han uppgav att han inte upplevde några visuella förändringar eller förbättringar i balans. Binokulär diplopi var fortfarande konstant; därför förblev det högra ögat patchat. Ögonsmärta med långt blickar och snabba ögonrörelser var fortfarande närvarande. Vid begränsad sängundersökning förblev bäst korrigerade visuella acuiteter 20/20 i höger och vänster ögon. Eleverna utvidgades vid 8.0mm i båda ögonen med minimal reaktivitet, vilket förbättrades något från dagen innan. Färgseendet var normalt i höger och vänster ögon. Extraokulära motiliteter var fulla i alla kvadranter med smärta som fortfarande finns på långt horisontella blickar. Horisontella sysselsättningar förblev saccadic med ryckiga rörelser och slutpunkt nystagmus. De optiska nerverna verkade friska med tydliga marginaler och ett kopp-skivförhållande på 0,15 i båda ögonen.
två dagar efter uppgav patienten en förbättring av alla symtom och att hans ögon ”mår bättre idag än de har varit på ett tag.”Ögonsmärta och binokulär diplopi löstes båda. Visuella acuities förblev 20/20 i höger och vänster ögon. Pupillstorlekarna var 7,5 mm i mörker och 7,0 mm i ljus med förbättrade direkta och konsensuella svar i båda ögonen. Extraokulära motiliteter var fulla i alla kvadranter utan ögonsmärta. Horisontella sysselsättningar förblev saccadic med ryckiga rörelser och slutpunkt nystagmus. Neurologisk undersökning avslöjade onormala reflexer, som förblev stabila. Behandlingsalternativen för MFS inkluderar plasmaferes och intravenöst (IV) immunoglobulin IgG, men dessa hölls kvar med tanke på förbättringen av oftalmoplegi och ataxi.
fyra dagar senare rapporterade patienten att alla symtom fortfarande förbättrades, med vissa svårigheter att fokusera och spåra när du använder datorn. Balansen var 80% löst och det fanns få förekomster av distansdiplopi. Acuities förblev 20/20 OU. Eleverna var 5,5 mm i mörker och 4,0 mm i ljus med 3+ direkta och konsensuella svar OU. Extraokulära motiliteter var fulla i alla kvadranter utan ögonsmärta. Horisontella sysselsättningar förbättrades, utan saccadic rörelser. Monokulärt boende var normalt, vilket mättes 8,5 respektive 9 prisma dioptrar OD respektive OS.
en vecka senare rapporterade patienten att hans syn återvände till nästan normal utan diplopi och milda svårigheter att fokusera och spåra. Balansen var 100% löst. Visuella acuities förblev 20/20 i höger och vänster ögon. Pupillstorlekarna var 5,5 mm i mörker, 4,0 mm i ljus med 4 + direkta och konsensuella svar OU. Extraokulära motiliteter var fulla i alla kvadranter utan ögonsmärta. Horisontella sysselsättningar förbättrades utan observerade saccadic rörelser. Okulär hälsa var unremarkable OU.
behandlingen avbröts med tanke på upplösningen av oftalmoplegi och ataxi med stabil areflexi. Full återhämtning av oftalmoplegi och ataxi tog två veckor. Ledningen inkluderade noggrann övervakning och uppföljning på fyra veckor; patienten rekommenderades att återvända tidigare om något av hans symtom återvände.
kliniska egenskaper
i väl beskrivna studier av MFS fick alla patienter den kliniska triaden av oftalmoplegi, ataxi och areflexi.4,5 symtomdebut uppträder vanligtvis under flera dagar, och patienter lider av en virusinfektion en till fyra veckor före starten av kliniska symtom.4,5 enligt en studie av 50 patienter med tillståndet är medelintervallet mellan infektionsuppkomst och utveckling av neurologiska symtom åtta dagar.4 andra tecken på MFS inkluderar sluddrigt tal, svårigheter att svälja och ett onormalt ansiktsuttryck med oförmåga att le eller vissla.
oftalmologiska egenskaper. Utövare bör vara på jakt efter mydriasis, lockretraktion, spetsig vinkelstängning och diplopi sekundärt till nervpalsier som påverkar CN III, IV och VI.3,8,10,22,24 diplopi är det vanligaste oftalmologiska symptom som rapporterats i många MFS-studier.8,16,25,26,27 diplopi är också det första symptom som rapporterades hos 38,6% av 223 patienter i en landmärkestudie och 65% av 466 patienter i en andra studie.8,27 i den andra studien uppvisade 100% av patienterna extern oftalmoplegi, medan intern oftalmoplegi var närvarande hos 35% av patienterna.27 extern oftalmoplegi avser försämring av yttre extraokulära muskler. Intern oftalmoplegi avser försämring av pupillärsfinktern och ciliarmuskeln. Komplett oftalmoplegi påverkar både yttre och inre muskler.
i en retrospektiv studie av 19 patienter med MFS presenterades alla med en eller flera nervpalsier som påverkar de extraokulära musklerna.25 andra studier visar att MFS-patienter kan uppleva flera kranialnervpalsier, vilket kan manifesteras bilateralt.22,24,25 ett vanligt fynd som finns bland anti-GQ1b IGG-positiva störningar är bortföringsunderskott som överensstämmer med en ensidig eller bilateral cn VI pares.26,28 intern oftalmoplegi orsakar pupillmydriasis, där pupillkontraktion till ljus och / eller nära stimulering kan sträcka sig från minimal till frånvarande.8,26 i en rapport var mydriasis närvarande hos 42% av patienterna. Inblandning av CN VII inträffade hos cirka 45,7% av MFS-patienterna som orsakade ansiktssvaghet, oförmåga att le eller vissla.8
ataxi. Orsaken till denna kliniska egenskap hos MFS är inte helt förstådd. Debatt finns om ataxi orsakas av dysfunktion centralt i cerebellum eller perifert. Den första hypotesen, föreslagen av Dr.Fisher, postulerade involveringen av Ia-afferenta neuroner.2 detta stöddes av en andra studie årtionden senare, som visade abnormiteter hos Ia-afferenta fibrer i MFS.11 onormal perifer nervinvolvering har också föreslagits med en obalans mellan proprioceptiv inmatning från muskelspindlar och kinestetisk information från gemensamma receptorer.12
det har också funnits stödjande bevis för att ataxi har sitt ursprung i cerebellum. En övervägande av anti-GQ1b IgG-antikropp i cerebellum hittades med användning av immunocytokemisk färgning av humant cerebellum och bekräftades ytterligare med western blot-studier, som visade ökad anti-GQ1b IgG-antikropp hos MFS-patienter jämfört med kontroll, även om mekanismen för cerebellär involvering inte har studerats.13,14 år 2015 publicerade forskare en fallrapport om en MFS-patient som genomgick MR. Det fanns ett reducerat n-acetylaspartat / kreatinförhållande, vilket tyder på cerebellär dysfunktion, som återvände till normala 2,5 månader efter återhämtning.23
areflexi. Denna kliniska egenskap, tillsammans med depression av djupa tendonreflexer, är ett tecken på involvering av perifert nervsystem i MFS. Elektrofysiologiska studier har validerat onormal perifer nervledning i GBS och MFS.3 i en studie presenterade 81,6% av MFS-Fallen arefexia.8 En annan landmärkestudie visade att alla patienter upplevde areflexi, som fortfarande var närvarande sex månader efter starten.4
hur vanligt är MFS?
epidemiologiska data om Miller Fishers syndrom är begränsade. Förekomsten av MFS är ganska sällsynt och förekommer hos 0,09 per 100 000 personer årligen.3 MFS förekommer oftare hos patienter med Guillain-Barr Xiai syndrom, från 3% till 25%.4,6,7 denna förening förekommer mer hos patienter med Fjärran Östern härkomst, vilket tyder på en möjlig genetisk komponent till MFS. Medelåldern för början är 43, med ett intervall på 13 till 78,5 MFS påverkar män dubbelt så mycket som kvinnor med ett förhållande på två till 1,03,5 MFS förekommer mer under vinter-och vårsäsongerna.5,6,8 den exakta orsaken till säsongsberoende har inte fastställts, men är sannolikt associerad med tillståndets postinfektiösa natur, eftersom bakteriella och virusinfektioner har visat sig utlösa ett autoimmunt svar som orsakar produktion av anti-GQ1b IgG-antikroppen i MFS.
patofysiologi
patofysiologin för Miller Fishers syndrom är inte väl förstådd; emellertid finns flera hypoteser från immunologiska och histologiska studier. Det är väl känt att tillståndet ligger inom spektrumet av anti-GQ1b IGG-antikroppssyndrom tillsammans med Guillain-Barr-Xiais syndrom och Bickerstaffs hjärnstamsencefalit. gangliosiden GQ1b är en grupp komplexa lipider som är involverade i centrala och perifera nervsystemet. GQ1b är en komponent i plasmamembranstrukturen i kranialnerver som levererar de extraokulära musklerna och är involverad i cellfunktionen vid den presynaptiska neuromuskulära korsningen.
en autoimmun mekanism från en föregående utlösande infektion kommer att producera anti-GQ1b IgG-antikroppen, som skadar gangliosid gq1b-funktionen och orsakar demyelinering. Histologiska studier har visat demyelinering och axonal svullnad i perifera och oculomotoriska kranialnerver.15 Anti-GQ1bIgG-antikroppen är frånvarande hos friska patienter, men positiv hos över 90% av patienterna med MFS.16,25
bakteriella och virala infektioner har visat sig utlösa ett autoimmunt svar, vilket orsakar produktion av anti-GQ 1b IgG-antikroppen. Följande infektionsmedel som har associerats med MFS inkluderar mykoplasma lunginflammation, HIV, Campylobacter jejuni, Hemophilus influensa, Helicobacter pylori och Epstein-Barr-virus.4,16 i en rapport som tittade på 466 MFS-patienter hade 90% en antecedent sjukdom, inklusive övre luftvägsinfektion, diarre eller båda.27
prognos och behandling
Miller Fisher syndrom är en självbegränsande sjukdom och har en övergripande positiv prognos. Symtomen förbättras vanligtvis efter några veckor med full återhämtning som vanligtvis förekommer inom två till tre månader. I en studie började återhämtningen med en median på 13 dagar från symptomstart, och fullständig upplösning av oftalmoplegi och ataxi inträffade på sex månader.4,5 återfall har visat sig förekomma i mindre än 3% av fallen.4,5
Även om MFS vanligtvis är självbegränsande har systemiska komplikationer associerats med tillståndet. Övre luftvägsinfektioner har hittats hos 56% till 76% av MFS-patienterna, vilket kan utvecklas till andningssvikt som kräver mekanisk ventilation.4,18,19 andra sällsynta allvarliga komplikationer inkluderar kardiomyopati, laktacidos och koma.3,20
behandlingsalternativen för MFS inkluderar plasmaferes, IV immunoglobulin IgG och övervakning utan behandling. Forskare postulerar att plasmaferes och IV IgG kan vara effektiva för att påskynda upplösningstiden eftersom antikropp Gq1b är IgG i klassen och halveringstiden för IgG är ungefär 21 dagar, vilket är längre än de fem till sex dagars halveringstiderna för IgM och Iga.19 emellertid har inga randomiserade dubbelblindade placebokontrollerade studier som undersöker dessa behandlingar genomförts.
en retrospektiv studie misslyckades med att visa plasmaferes förändrade risken för fullständig återhämtning och tiden för att lösa ataxi och oftalmoplegi; vidare påverkade intervallet från början till början av plasmaferesbehandling inte tiden till upplösning eller svårighetsgraden av symtom vid början. En fallrapport indikerar emellertid att plasmaferes indikeras när djup ataxi, motorisk och andningsstörning är närvarande.21
patienter bör övervakas noggrant med avseende på risk för allvarliga systemiska komplikationer såsom övre andningssvikt. Studier visar ingen signifikant förbättring av återhämtningstiden med IV IgG eller plasmaferesbehandling i MFS, så övervakning kan vara en utövares bästa alternativ.
även om det är sällsynt behöver tillståndet inte bli odiagnostiserat. Genom att känna igen de viktigaste kliniska egenskaperna kan utövare avslöja orsaken till patientens symtom och få förtroende för en fullständig återhämtning.
Drs Wang och Cantrell är personaloptiker vid Orlando VA Medical Center. Dr. Cali är personaloptiker vid Lee County VA Clinic. Författarna vill tacka Joseph Miller, od, Paul Gruosso, OD och Vanessa Santos, OD, för hjälp med detta manuskript.
1. Collier J. perifer neurit: Morisa-föreläsningarna. Edinburgh Med J. 1932:39: 601-18.
2. Fisher M. en ovanlig variant av akut idiopatisk polyneurit (syndrom oftalmoplegi, ataxi och areflexi). N Eng J Med. 1956:255:57-65.
3. Lo YL, et al. Kliniskt och immunologiskt spektrum av Miller Fishers syndrom. Muskel Nerv. 2007:36(5):615-27.
4. Mori M, Kuwabara S, Fukutake T, et al. Kliniska egenskaper och prognos för Miller Fisher syndrom. Neurology. 2001:56(8): 1105-6.
5. Mori M, Kuwabara S, Fukutake T, et al. Plasmafaresis och Miller Fisher syndrom: analys av 50 på varandra följande fall. J Neurol Neurosurg Psych. 2002:72:680.
6. Yuan CL, Wang YJ, Tsai CP. Miller Fisher syndrom: en sjukhusbaserad retrospektiv studie. Euro J Neurol. 2000:44(2):79-85.
7. Cheng BC, Chang WN, Chang CS et al. Guillain-Barr Xiai syndrom i södra Taiwan: kliniska egenskaper, prognostiska faktorer och terapeutiska resultat. Euro J Neurol. 2003:10 (6):655-62.
8. Berlit P, Rakicky J. Miller Fishers syndrom. Granskning av litteratur. J klinisk neuro-oftalmologi. 1992:12:57-63.
9. Lm, Cheng SY, et al. Guillain-Barr Xiai syndrom i Taiwan: en klinisk studie av 167 patienter. J Neurol Neurosurg Psych. 1997:63:494-500.
10. Tatsomoto M, Odaka M, Hirata K, Yuki N. isolerad abducens pares som en regional variant av Guillain-Barr Xiais syndrom. J Neurol Sci. 2006:243:35-8.
11. Weiss JA, Vit JC. Korrelation av 1a afferent ledning med ataxi av Fisher syndrom. Muskel Nerv. 1986:9:327-32.
12. Das P, Biswash S, et al. Miller Fisher-variant av guillain-Barr Bisexuell syndrom: en fallrapport och klinisk granskning. Bangabandhu Sheikh Mujib Medical Univer J. 2012: 5 (1):69-71
13. Det finns många olika typer av produkter. Selektiv färgning av det cerebellära molekylära skiktet med serum IGG av Miller Fisher och relaterade syndrom. Neurology. 1996:47:1317-20.
14. Inoue N, Koh C, Iwahashi T. detektion av serumanticerebellära antikroppar hos patienter med Miller Fishers syndrom. Euro J Neurol. 1999:42:230-4.
15. Barontini F, Di Lollo S, Maurri S, Lambruschini P. lokalisering av den patologiska processen i Miller Fishers syndrom. Italien J Neurol Sci. 1992:13:221-5.
16. Koga M, Yuki N, Takahashi M, et al. Nära association av IgA-Anti-gangliosidantikroppar med antecedent Campylobacter jejuni-infektion i Guillain-Barr Audi och Fishers syndrom. J Neuroimmunol. 2003:141:112-7.
17. Guiloff RJ. Perifer nervledning i Miller Fisher syndrom. J Neurol Neurosurg Psychiat. 1977:40:801-7.
18. Han är en av de mest kända. Fördröjd motorisk och sensorisk neuropati hos en patient med hjärnstammens encefalit. J Neurol Sci. 2005:234:105-8.
19. Arakata Y, Yoshimuro M, Kobayashi S, et al. Användningen av intravenöst immunoglobulin i Miller Fisher syndrom. Hjärnan Utveckla J. 1993:15:231-3.
20. Matsumoto H, Kobayashi O, Tamura K, et al. Miller Fisher syndrom med övergående koma: jämförelse med bickerstaffs hjärnstammencefalit. Hjärnan Utveckla J. 2002:24: 98-101.
21. Ja, Chen WH, Chen JR, et al. Miller Fisher syndrom med centralt engagemang: framgångsrik behandling med plasmaferes. Therap Aferes Dialys J. 1999: 3: 69-71.
22. Papanikolaou T, Cath G, Boothman B, et al. Fallrapport: akut bilateral oftalmopares med pupilär areflexisk mydriasis i Miller-Fisher syndrom behandlat med intravenöst immunoglobulin. J Oftalmol. 2010; artikel-ID 291840.
23. Sandler RD, Hoggard N, Hadjivassiliou M. Miller-Fisher syndrom: är ataxi central eller perifer? Cerebellum Ataxias. 2015:2:3.
24. Ejma M, Waliszewska-Pros Asia m, Hofman A, et al. Progressivt subakut Miller-fisher syndrom behandlas framgångsrikt med plasmaferes. Polska J Neurol Neurosurg. 2015;49(2):137-8.
25. Det finns en hel del att välja mellan. Miller Fisher syndrom: 10 års erfarenhet i ett tredje nivåcenter. Euro Neurol. 2009; 62: 149-54
26. Snyder LA, Rismondo V, Miller NR. Fisher-varianten av Guillain-Barr Xiai syndrom (Fisher syndrom). J Neurooftalmol. 2009 Dec; 29 (4): 312-24.
27. Ito M, Kuwabara S, Odaka M, et al. Bickerstaffs hjärnstammens encefalit och fisher syndrom bildar ett kontinuerligt spektrum: klinisk analys av 581 fall. J Neurol. 2008;255:674-82.
28. Yuki N. akut pares av extraokulära muskler associerade med IgG anti-GQ1b-antikropp. Ann Neurol 1996; 39: 668-72.