Lågspänningsglaukom: en Oxymoron i oftalmologi
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (Visa författaranslutningar)
föreslagen citat för denna artikel: Costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. Lågspänningsglaukom: en Oxymoron i oftalmologi. Föregående Kronisk Dis 2019; 16: 180534. DOI:http://dx.doi.org/10.5888/pcd16.180534external ikon.
termen glaukom avser en grupp okulära tillstånd som kännetecknas av progressiv optisk nervskada och förlust av synfält (1). Glaukomatös optisk neuropati beror på den progressiva förlusten av retinala ganglionceller; förhöjt intraokulärt tryck (IOP) är en viktig riskfaktor. IOP kan agera direkt, genom mekanisk effekt eller indirekt genom att påverka blodtillförseln (2). Faktorer som påverkar progressionen av glaukomatös optisk neuropati inkluderar äldre ålder, avancerat stadium av sjukdom, högre IOP och skivblödningar (3). Hos patienter med primär öppenvinkelglaukom (POAG) är det ökade motståndet mot vattenutflöde genom det trabekulära nätverket den största skyldige för förhöjd IOP. Trots tillräcklig kontroll av IOP kan glaukomatös optisk neuropati ofta fortsätta att utvecklas. Således erkänns faktorer som inte är relaterade till IOP, med det viktigaste är en minskning av blodtillförseln till optisk nerv (4).
andra faktorer som inte är relaterade till IOP inkluderar glutamattoxicitet, oxidativ stress, autoimmunitet och vaskulär dysregulering (3). Glaukom med låg spänning (LTG) definieras som en form av glaukom som nära efterliknar POAG, men IOP-nivåer ligger inom det normala intervallet och den troliga patogenesen är vaskulär.
de kontroversiella frågorna är 1) är LTG en sjukdom på spektrumet av POAG (på vänster sida av fördelningen av IOP, på de lägsta nivåerna)?, 2) är det optiska skivans utseende sekundärt till optisk nervhypoperfusion på grund av kärlsjukdomar?, eller 3) bör LTG inkluderas i ett spektrum av medfödda och förvärvade optiska neuropatier som kan simulera glaukomatös optisk neuropati?
Top
är Lågspänningsglaukom en sjukdom på spektrumet av primär öppenvinkelglaukom?
När Albrecht von Graefe 1857 beskrev en form av glaukom som manifesterade skador på det optiska nervhuvudet och en öppen främre kammarvinkel, med IOP inom referensområdet, betraktades digital palpationstonometri som guldstandarden. Om han hade använt en intryckstonometer för att mäta IOP, skulle tonometriens stora brist ha varit att den förskjutit så mycket vätska vid kontakt med ögat att de uppmätta avläsningarna skulle vara mycket varierande och felaktiga. Omvänt, om han hade använt indragstonometri, skulle det inte ha beaktat felklassificeringen till följd av närvaron av en tunn central hornhinna (1). Många diagnoser av LTG var för ögon med tunna hornhinnor och baserades på falska låga värden för IOP, ett konstaterande som tvivlar på diagnosen LTG (5). Vidare måste frånvaron av förhöjd IOP hittas vid mätningar som utförs mer än en gång eller under dagtid, eftersom IOP visar dagliga och nattliga fluktuationer hos friska försökspersoner, och ännu mer hos patienter med POAG eller LTG (6). För variationer i IOP kan 3 populationer av LTG-patienter särskiljas: patienter utan IOP-fluktuationer, patienter med daglig IOP-akrofas (toppen eller toppen av en cykel) och patienter med nattlig IOP-akrofas (7). Patienter i de 2 sista kategorierna bör betraktas som sanna POAG-patienter snarare än LTG-patienter, hos vilka glaukomatös optisk neuropati uppträder trots normal IOP. Det är troligt att patienter med ett dagligt eller nattligt akrofas har registrerats i studier baserade på den mekaniska teorin; reduktion av IOP kan bromsa utvecklingen av synfältförlust endast hos dessa patienter (8). Data från Lågtrycksglaukombehandlingsstudien lyfte fram IOP: s roll i LTG-patogenes; progressionen av synfältförlust reducerades med 9,1% med timolol 0,5% och med 39,1% med brimonidin 0,2% efter 2 års behandling (8). I denna studie registrerades dock IOP-värden uteslutande under dagtid. Således, om patienter med ett sämre synfält hade IOP nattligt akrofas är okänt. Andra studier på asymmetrisk LTG rapporterade att ögat med högre IOP visar större glaukomatös skada än ögat med lägre IOP, vilket upprätthåller IOP: s roll i patogenesen (9). Men i alla dessa kliniska prövningar mättes IOP endast under kontorstid; således registrerades inte beteendet hos nattlig IOP. En ny studie där nychthemeral IOP-kurvor utvärderades med en telemetrisk sensor visade ett nattligt akrofas med IOP-spikar hos patienter med LTG, även om dessa spikar var på signifikant lägre nivåer än de spikar som hittades bland patienter med POAG (7). Denna studie rapporterade att IOP toppade på natten hos 40% till 80% av patienterna med glaukom med normal spänning, och mönstret hos dessa patienter liknade mönstret hos patienter med POAG. I 24-timmarskurvor hade patienter med LTG och POAG mer uttalade mönster av IOP på kvällen och natten än på morgonen, med fler toppar och större IOP-fluktuationer under natten än under kvällen (7). Andra faktorer kan bekräfta hypotesen om en primär IOP-relaterad mekanisk stress i LTG, såsom närvaron av förändringar i de vattenhaltiga humorutflödesvägarna som liknar dem som förekommer i POAG (10).
hos patienter där LTG kan betraktas som en sjukdom på spektrumet av POAG, måste diagnostiska och terapeutiska strategier som liknar dem för patienter med hyperbar glaukom genomföras med hjälp av en ögonläkare (figur).
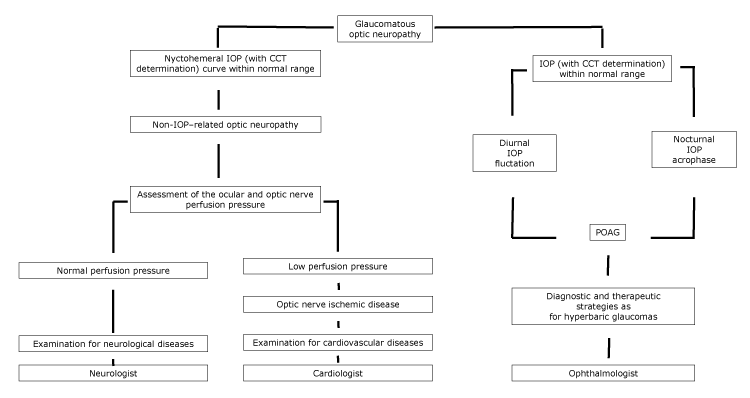
figur.
föreslaget flödesschema för optisk neuropati, med specialistreferens, enligt nychthemeral IOP-egenskaper. Förkortningar: CCT, Central hornhinnans tjocklek; IOP, intraokulärt tryck; POAG, primär öppenvinkelglaukom.
Top
är det optiska skivans utseende sekundärt till optisk Nervhypoperfusion på grund av kärlsjukdomar?
hos patienter med LTG och normala nychthemeral IOP-kurvor kan mekaniska faktorer inte vara ansvariga för optisk neuropati; tryckoberoende faktorer kan vara involverade, med vaskulära förändringar som potentiellt är de viktigaste (5). En glaukomatös optisk neuropati kan observeras hos patienter med en kardiovaskulär händelse i anamnesen eller med kronisk ateroskleros eller obstruktiva arteriella sjukdomar (11). Minskad blodflödeshastighet i retrobulbarartärer och i cerebral cirkulation, lågt diastoliskt blodtryck och mindre central retinal kärldiameter har också observerats hos patienter med LTG (5). Hos dessa patienter beror patogenesen av sjukdom på ett nedsatt okulärt perfusionstryck, huvudsakligen kopplat till primär vaskulär dysregulering eller till en generaliserad dysfunktion i endotel-eller autonoma nervsystemet (5,11). Det är emellertid oklart om dessa faktorer var orsaken eller resultatet av optisk neuropati. Ur klinisk synvinkel visar LTG en högre förekomst av skivblödningar och är oftare förknippad med kärlsjukdomar som migrän, obstruktiv sömnapnea eller Raynauds syndrom än med IOP (5). Slutligen visar ungefär hälften av LTG-patienter med pre-perimetrisk sjukdom skadeprogression trots normala IOP-värden (12). Alla dessa resultat tyder på den viktiga rollen som vaskulär dysregulering.
hos patienter med hjärt-kärlsjukdomar kan optisk skivkoppning tendera att inte utvecklas om den bakomliggande orsaken till optisk neuropati har kontrollerats. Dessutom kan LTG-patienter visa cirkumpapillär atrofi såväl som cerebrala kortikala mikroinfarkter, vilka är tecken på ischemi (5). Hos patienter där kärlsjukdomar inducerar en optisk nervhypoperfusion måste en fullständig diagnostisk undersökning för hjärt-kärlsjukdomar utföras med hjälp av en kardiolog (figur).
Top
bör LTG inkluderas i ett spektrum av medfödda och förvärvade optiska neuropatier som kan simulera en Glaukomatös optisk neuropati?
när de mer frekventa orsakerna till optisk skivkoppning har uteslutits, bör möjligheten till neurodegenerativ optisk neuropati övervägas. Dessa fall är de mest frustrerande, eftersom optisk skivskada fortskrider även efter att IOP har sänkts. Många medfödda och förvärvade optiska neuropatier ingår i denna grupp av fall, och differentiering mellan glaucomatous och nonglaucomatous cupping kan vara utmanande även för erfarna observatörer (13). Bland de medfödda formerna av optisk skivkoppning, megalopapilla, autosomal dominant optisk atrofi och Leber ärftlig optisk neuropati kan producera en optisk skivutgrävning som simulerar glaukomatös optisk neuropati.
de förvärvade neuropatierna kan vara sekundära till inflammatoriska, komprimerande, toxiska och traumatiska orsaker. Optisk neurit kan ge en ökning av kopp-till-skivförhållandet som, även om det är ensidigt, kan förväxlas med glaukomatös optisk neuropati. Kompressionsskador inklusive meningiom, hypofysadenom, kraniopharyngiom och inre karotisartäraneurysm kan leda till asymmetrisk optisk skivkoppning och felaktigt tillskriven LTG. Metanol-och etambutolförgiftning kan ge en bilateral optisk skivkoppning som liknar glaukomatös optisk neuropati, sekundär till axonal förlust. Således, när en asymmetrisk förstorad kopp observeras, är ytterligare neuro-oftalmologisk undersökning nödvändig (13).
slutligen, bland förhållanden som leder till optisk skivkoppning, har åldrande en huvudroll. Harju et al fann att graden av optisk skivkoppning ökade hos friska äldre studiedeltagare på grund av fysiologisk fiberförlust. Deras studiepopulation var lämplig och representerade en uppsättning friska ögon utan glaukom; under 11 års uppföljning utvecklade inga studiedeltagare synfältförändringar och ingen signifikant ökning av IOP registrerades (14). I det senare fallet måste en fullständig diagnostisk undersökning för neurologiska sjukdomar utföras med hjälp av en neurolog (figur).
förbättringar i diagnostiska tekniker gör det lättare än tidigare att klassificera optisk skivkoppning; en beskrivning av optiska skivans egenskaper i kombination med avbildning av retinal nervfiberskiktet och optisk skivtopografi möjliggör differentiering mellan glaucomatös och nonglaucomatös optisk skivkoppning. Dessutom hjälper en noggrann analys av patienthistoria, tillsammans med morfologisk och funktionell bedömning av optisk nerv, att identifiera störningar.
termen LTG kan vara en oxymoron, ett nostalgiskt minne från det förflutna när en definierad diagnos inte var möjlig. Att använda termen är som att använda ordet ”feber”när det inte finns någon hög temperatur eller säga festina lente (”mer brådska, mindre hastighet”). Termen LTG kan vara vilseledande eller felaktig, eftersom den hänvisar till ett mekaniskt problem med IOP, medan optisk skivkoppning och synfältförlust i ögon med normalt intraokulärt tryck orsakas av andra faktorer. Därför, i närvaro av optisk skivkoppning med normal IOP, bör ögonläkare undersöka andra troliga orsaker till optisk nervskada förutom intraokulärt tryck.
Top
erkännanden
denna studie fick inget specifikt bidrag från någon finansieringsbyrå inom offentliga, kommersiella eller ideella sektorer.
topp
författarinformation
motsvarande författare: Luca Agnifili, MD, PhD, Oftalmologiklinik, Via Dei Vestini, 66100, Chieti (CH), Italien. Telefon: +39-0871-358489. E-post: [email protected].
Författartillhörighet: 1avdelningen för medicin och hälsovetenskap, universitetet i Molise, Campobasso, Italien. 2avdelningen för medicin och åldrande vetenskap, Oftalmologiklinik, universitet G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14-21. Crossrefextern ikon Pubmedextern ikon
- de Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; studiegrupp för behandling av glaukom med lågt tryck. Riskfaktorer för synfältprogression i studien för behandling av glaukom med lågt tryck. Am J Oftalmol 2012; 154 (4):702-11. Crossrefextern ikon Pubmedextern ikon
- Cartwright MJ, Anderson Dr. korrelation av asymmetrisk skada med asymmetriskt intraokulärt tryck i glaukom med normal spänning (glaukom med låg spänning). Arch Oftalmol 1988; 106 (7):898-900. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top