Low-Napětí Glaukom: oxymóron v Oftalmologii
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (Pohled autora orientace)
Navrhl citace pro tento článek: Costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. Low-Napětí Glaukom: oxymóron v Oftalmologii. Předchozí Dis 2019; 16:180534. DOI: http://dx.doi.org/10.5888/pcd16.180534external icon.
termín glaukom označuje skupinu očních stavů charakterizovaných progresivním poškozením zrakového nervu a ztrátou zorného pole (1). Glaukomatózní optická neuropatie je způsobena progresivní ztrátou gangliových buněk sítnice; zvýšený nitrooční tlak (IOP) je jedním z hlavních rizikových faktorů. IOP může působit přímo mechanickým účinkem nebo nepřímo ovlivněním přívodu krve (2). Faktory, které ovlivňují progresi glaukomatózní optické neuropatie, zahrnují vyšší věk, pokročilé stadium onemocnění, vyšší IOP a krvácení z disku (3). U pacientů s primárním glaukomem s otevřeným úhlem (POAG), zvýšená odolnost vůči vodným odliv přes trámčiny je hlavním viníkem zvýšené IOP. I přes adekvátní kontrolu IOP však může glaukomatózní optická neuropatie často pokračovat. Jsou tedy rozpoznány faktory, které nesouvisejí s IOP, přičemž nejdůležitější je snížení přívodu krve do optického nervu (4).
Další faktory nesouvisející s IOP zahrnují toxicitu glutamátu, oxidační stres, autoimunitu a vaskulární dysregulaci (3). Glaukom s nízkým napětím (LTG) je definován jako forma glaukomu, která úzce napodobuje POAG, ale hladiny IOP jsou v normálním rozmezí a pravděpodobná patogeneze je vaskulární.
kontroverzní otázky jsou 1) je LTG onemocnění na spektrum POAG (na levé straně distribuce IOP, na nejnižších úrovních)?, 2) je vzhled optického disku sekundární k hypoperfuzi optického nervu v důsledku vaskulárních onemocnění?, nebo 3) měl by být LTG zahrnut do spektra vrozených a získaných optických neuropatií, které mohou simulovat glaukomatózní optickou neuropatii?
Top
je glaukom s nízkým napětím onemocnění ve spektru primárního glaukomu s otevřeným úhlem?
Když v roce 1857 Albrecht von Graefe popsána forma glaukom projevuje poškození zrakového nervu a otevřeného úhlu přední komory, s IOP v rámci referenčního rozsahu, digitální palpace tonometrie byla považována za zlatý standard. Pokud měl dojem, tonometr k měření nitroočního tlaku, hlavní nedostatek tonometrie by bylo, že to vysídlených tolik tekutiny při styku s okem, že naměřené hodnoty by být vysoce variabilní a nepřesné. Naopak, pokud by použil tonometrii odsazení, nezohlednil by nesprávnou klasifikaci vyplývající z přítomnosti tenké centrální rohovky (1). Mnoho diagnóz LTG bylo pro oči s tenkými rohovkami a bylo založeno na falešně nízkých hodnotách pro IOP, což je zjištění, které zpochybňuje diagnózu LTG (5). Kromě toho, absence zvýšeného nitroočního tlaku, musí být nalezen na měření provádí více než jednou, nebo během dne, protože IOP ukazuje, denní a noční výkyvy u zdravých jedinců a ještě větší u pacientů s POAG nebo LTG (6). Pro variace IOP lze rozlišit 3 populace pacientů s LTG: pacienti bez fluktuací IOP, pacienti s denní IOP akrofázou (hřeben nebo vrchol cyklu) a pacienti s noční IOP akrofázou (7). Pacienti ve 2 posledních kategoriích by měli být považováni za skutečné pacienty POAG spíše než za pacienty s LTG, u nichž se glaukomatózní optická neuropatie vyskytuje i přes normální IOP. Je pravděpodobné, že pacienti s denní nebo noční akrofázou byli zařazeni do studií založených na mechanické teorii; snížení IOP může zpomalit progresi ztráty zorného pole pouze u těchto pacientů (8). Data z Nízkého Tlaku, Glaukom Léčba Studie zdůraznily roli IOP v LTG patogenezi, progresi ztráty vizuálního pole byla snížena o 9,1% s timololem 0,5% a o 39,1% s brimonidin 0.2% po 2 letech léčby (8). V této studii však byly hodnoty IOP zaznamenány výhradně během dne. Není tedy známo, zda pacienti s horším zorným polem měli noční akrofázu IOP. Jiné studie asymetrického LTG uváděly, že oko s vyšším IOP vykazuje větší glaukomatózní poškození než oko s nižším IOP, což udržuje roli IOP v patogenezi (9). Přesto ve všech těchto klinických studiích byl IOP měřen pouze během úředních hodin; chování nočního IOP tedy nebylo zaznamenáno. Nedávná studie, ve které nychthemeral IOP křivky byly vyhodnoceny s telemetrické čidlo ukázal, noční acrophase s IOP hroty u pacientů s LTG, i když tyto hroty byly na podstatně nižší úrovni než hroty nalezeny u pacientů s POAG (7). Tato studie uvádí, že IOP dosáhla vrcholu v noci u 40% až 80% pacientů s glaukomem s normálním napětím a vzorec u těchto pacientů byl podobný vzoru u pacientů s POAG. Ve 24hodinových křivkách měli pacienti s LTG a POAG výraznější vzorce IOP večer a noc než ráno, s více vrcholy a větší fluktuací IOP během noci než večer (7). Další faktory mohou potvrdit hypotézu, že primární IOP-související mechanické namáhání v LTG, jako je přítomnost změn v komorové odliv cesty podobné těm, které se objevují v POAG (10).
U pacientů, kde LTG může být považována za nemoc na spektrum POAG, diagnostické a terapeutické strategie podobné těm, pro pacienty s hyperbarická glaukom musí být realizován s pomocí očního lékaře (viz Obrázek).
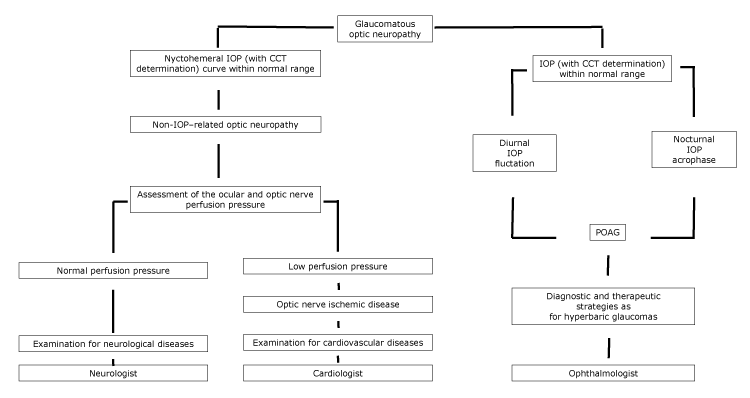
obrázek.
navrhovaný vývojový diagram optické neuropatie s doporučením specialisty podle charakteristik NYCHTHEMERAL IOP. Zkratky: CCT, tloušťka centrální rohovky; IOP, nitrooční tlak; POAG, primární glaukom s otevřeným úhlem.
Top
je vzhled optického disku sekundární k hypoperfuzi optického nervu v důsledku vaskulárních onemocnění?
u pacientů s LTG a normálními nychthemerálními křivkami IOP nemohou být za optickou neuropatii odpovědné mechanické faktory; mohou být zapojeny faktory nezávislé na tlaku, přičemž potenciálně nejdůležitější jsou vaskulární změny (5). Glaukomatózní optická neuropatie může být pozorována u pacientů s anamnézou kardiovaskulární příhody nebo s chronickou aterosklerózou nebo obstrukčními arteriálními chorobami (11). Snížená rychlost proudění krve v retrobulbární tepen a mozkové cirkulace, nízký diastolický krevní tlak, a menší centrální sítnice plavidla průměru byly také pozorovány u pacientů s LTG (5). U těchto pacientů, patogeneze onemocnění je způsobeno poruchou oční perfuzní tlak, především v souvislosti s primární cévní dysregulaci nebo generalizované dysfunkce endotelu nebo autonomního nervového systému (5,11). Není však jasné, zda tyto faktory byly příčinou nebo výsledkem optické neuropatie. Z klinického hlediska, LTG ukazuje vyšší výskyt disk krvácení a je častěji spojena s vaskulární onemocnění, jako je migréna, obstrukční spánková apnoe, nebo raynaudova syndromu, než s IOP (5). Nakonec asi polovina pacientů s LTG s preperimetrickým onemocněním vykazuje progresi poškození navzdory normálním hodnotám IOP (12). Všechna tato zjištění naznačují důležitou roli vaskulární dysregulace.
u pacientů s kardiovaskulárními chorobami může mít baňkování optického disku tendenci nepokračovat, pokud byla základní příčina optické neuropatie kontrolována. Pacienti s LTG mohou navíc vykazovat circumpapilární atrofii i mozkové kortikální mikroinfarkty, což jsou příznaky ischémie (5). U pacientů, u kterých cévní onemocnění indukují hypoperfuzi zrakového nervu, musí být provedeno kompletní diagnostické vyšetření kardiovaskulárních onemocnění s pomocí kardiologa (obrázek).
Top
měl by být LTG zahrnut do spektra vrozených a získaných optických neuropatií, které mohou simulovat glaukomatózní optickou neuropatii?
pokud byly vyloučeny častější příčiny baňkování optického disku, měla by být zvážena možnost neurodegenerativní optické neuropatie. Tyto případy jsou nejvíce frustrující, protože poškození optického disku postupuje i po snížení IOP. Mnoho vrozených a získaných optické neuropatie jsou zahrnuty v této skupině případů, a diferenciace mezi glaukomové a nonglaucomatous baňkování může být náročné i pro zkušené pozorovatele (13). Mezi vrozené formy optického disku baňkování, megalopapilla, autozomálně dominantní optická atrofie, a Leberovu hereditární optická neuropatie mohla vytvořit optický disk výkopové simulující glaukomové optické neuropatie.
získané neuropatie mohou být sekundární k zánětlivým, kompresním, toxickým a traumatickým příčinám. Optická neuritida může způsobit zvýšení poměru pohár-disk, který, i když jednostranný, může být zaměňován s glaukomatózní optickou neuropatií. Tlaková léze včetně meningeom, adenom hypofýzy, kraniofaryngeomem a vnitřní krční tepny aneurysma může vést k asymetrické optické disky baňkování a mylně přičítána LTG. Otrava methanolem a ethambutolem může způsobit bilaterální baňkování optického disku podobné glaukomatózní optické neuropatii, sekundární k axonální ztrátě. Když je tedy pozorován asymetrický zvětšený pohár, je nutné další neuro-oftalmologické vyšetření (13).
konečně, mezi podmínkami vedoucími k baňkování optických disků má stárnutí hlavní roli. Zjistili, že stupeň baňkování optického disku se zvýšil u zdravých starších účastníků studie kvůli fyziologické ztrátě vláken. Jejich studijní populace bylo vhodné a představuje sadu zdravé oči bez zákalu; po 11 letech sledování, žádná studie účastníci rozvinuté změny zorného pole, a žádný významný nárůst v IOP byl zaznamenán (14). V tomto druhém případě musí být provedeno kompletní diagnostické vyšetření neurologických onemocnění pomocí neurologa(obrázek).
Vylepšení v diagnostické techniky, aby bylo snadnější než kdykoli předtím zařadit optický disk baňkování; popis optického disku vlastnosti v kombinaci s zobrazení retinálních nervových vláken vrstva a optický disk topografie umožňuje diferenciaci mezi glaukomové a nonglaucomatous optického disku baňkování. Kromě toho pečlivá analýza anamnézy pacienta spolu s morfologickým a funkčním hodnocením zrakového nervu pomáhá identifikovat poruchy.
termín LTG by mohl být oxymoron, nostalgická vzpomínka na minulost, kdy definovaná diagnóza nebyla možná. Použití termínu je jako použití slova „horečka“, když není vysoká teplota nebo říká festina lente („více spěchu, méně rychlosti“). Termín LTG může být zavádějící nebo nepřesný, protože se týká mechanického problému IOP, zatímco baňkování optického disku a ztráta zorného pole v očích s normálním nitroočním tlakem jsou způsobeny jinými faktory. Proto v přítomnosti baňkování optického disku s normálním IOP by oftalmologové měli kromě nitroočního tlaku zkoumat další věrohodné příčiny poškození optického nervu.
Top
poděkování
tato studie neobdržela žádný konkrétní grant od žádné finanční agentury ve veřejném, komerčním nebo neziskovém sektoru.
Top
Informace o Autorovi
Odpovídající Autor: Luca Agnifili, MD, PhD., Oční Klinika, Via dei Vestini, 66100, Chieti (CH), Itálie. Telefon: + 39-0871-358489. E-mail: [email protected].
Autor Příslušnost: 1Department of Medicine and Health Sciences, University of Molise, Campobasso, Itálie. 2oddělení medicíny a vědy o stárnutí, oční klinika, Univerzita G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14-21. Crossrefexterní ikona Pubmedexterní ikona
- De Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; studie skupiny pro léčbu glaukomu s nízkým tlakem. Rizikové faktory progrese zorného pole ve studii léčby nízkotlakého glaukomu. Am J Oftalmol 2012; 154 (4): 702-11. Crossrefexterní ikona Pubmedexterní ikona
- Cartwright MJ, Anderson DR. korelace asymetrického poškození s asymetrickým nitroočním tlakem u glaukomu s normálním napětím (glaukom s nízkým napětím). Arch Ophthalmol 1988; 106 (7): 898-900. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top