De baixa Tensão Glaucoma: Um Oxímoro em Oftalmologia
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (Vista do autor afiliações)
citação Sugerida para este artigo: Costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. de Baixa Tensão Glaucoma: Um Oxímoro em Oftalmologia. Prev Chronic Dis 2019; 16: 180534. DOI: http://dx.doi.org/10.5888/pcd16.180534external icon.o termo glaucoma refere-se a um grupo de condições oculares caracterizadas por lesão progressiva do nervo óptico e perda do campo visual (1). A neuropatia óptica glaucomatosa é devida à perda progressiva de células de ganglionamento da retina; a pressão intra-ocular elevada (PIO) é um dos principais factores de risco. A PIO pode agir diretamente, por um efeito mecânico, ou indiretamente, influenciando o suprimento sanguíneo (2). Fatores que influenciam a progressão da neuropatia óptica glaucomatosa incluem idade mais avançada, estágio avançado da doença, alta pio, e hemorragias no disco (3). Em doentes com glaucoma primário de ângulo aberto (POAG), o aumento da resistência à saída aquosa através da malha trabecular é o principal culpado pela pio elevada. No entanto, apesar do controlo adequado da PIO, a neuropatia óptica glaucomatosa pode frequentemente continuar a progredir. Assim, fatores não relacionados com a PIO são reconhecidos, sendo o mais importante uma diminuição no fornecimento de sangue para o nervo óptico (4).outros factores não relacionados com a PIO incluem toxicidade do glutamato, stress oxidativo, autoimunidade e desregulação vascular (3). Glaucoma de baixa tensão (LTG) é definida como uma forma de glaucoma que imita de perto POAG, mas os níveis de Pio estão dentro do intervalo normal e a patogênese provável é vascular.
as questões controversas são 1) LTG é uma doença no espectro de POAG (no lado esquerdo da distribuição da PIO, nos níveis mais baixos)?, 2) a aparência do disco óptico é secundária à hipoperfusão do nervo óptico devido a doenças vasculares?, ou 3) O LTG deve ser incluído num espectro de neuropatias ópticas congénitas e adquiridas que possam simular neuropatia óptica glaucomatosa?o Glaucoma de baixa tensão é uma doença no espectro do Glaucoma primário de ângulo aberto?quando em 1857 Albrecht von Graefe descreveu uma forma de glaucoma manifestando danos na cabeça do nervo óptico e um ângulo aberto da câmara anterior, com pio dentro do intervalo de referência, a tonometria da palpação digital foi considerada o padrão-ouro. Se ele tivesse usado um tonômetro de impressão para medir a PIO, a grande deficiência da tonometria teria sido que ele deslocou tanto fluido em contato com o olho que as leituras medidas seriam altamente variáveis e imprecisas. Inversamente, se ele tivesse usado a tonometria de indentação, ela não teria considerado a desclassificação resultante da presença de uma córnea Central fina (1). Muitos diagnósticos de LTG foram para olhos com córneas finas e foram baseados em falsos valores baixos para a IOP, um achado que lança algumas dúvidas sobre o diagnóstico de LTG (5). Além disso, a ausência de Pio elevado deve ser encontrada em medições realizadas mais de uma vez ou durante o dia, uma vez que a PIO mostra flutuações diurnas e nocturnas em indivíduos saudáveis, e ainda mais em pacientes com POAG ou LTG (6). Para variações na pio, podem distinguir-se 3 populações de doentes com GTL: doentes sem flutuações da PIO, doentes com acrofase da Pio Diurna (crista ou pico de um ciclo) e doentes com acrofase da PIO nocturna (7). Os doentes nas 2 últimas categorias devem ser considerados doentes com POAG verdadeiros e não doentes com LTG, nos quais ocorre neuropatia óptica glaucomatosa, apesar da PIO normal. É provável que os doentes com acrofase diurna ou nocturna tenham sido incluídos em estudos baseados na teoria mecânica.; a redução da PIO pode retardar a progressão da perda do campo visual apenas nestes doentes (8). Dados de Baixa Pressão, o Tratamento de Glaucoma Estudo destacou o papel do IOP em LTG patogênese; a progressão da perda de campo visual foi reduzido 9,1% com timolol 0,5% e 39,1%, com brimonidina a 0,2%, após 2 anos de tratamento (8). No entanto, neste estudo, os valores da PIO foram registados exclusivamente durante o dia. Assim, desconhece-se se os doentes com um pior campo visual tinham acrofase noturna IOP. Outros estudos sobre o LTG assimétrico relataram que o olho com pio superior mostra maior dano glaucomatoso do que o olho com pio inferior, o que sustenta o papel do IOP na patogênese (9). No entanto, em todos estes ensaios clínicos, a Pio foi medida apenas durante as horas de expediente; assim, o comportamento da PIO noturna não foi registrado. Um estudo recente no qual as curvas nychthemeral IOP foram avaliadas com um sensor telemétrico mostrou uma acrofase noturna com picos IOP em pacientes com LTG, embora estes picos estivessem em níveis significativamente mais baixos do que os picos encontrados em pacientes com POAG (7). Este estudo relatou que a PIO atingiu um pico noturno em 40% a 80% dos pacientes com glaucoma de tensão normal, e o padrão nestes pacientes foi semelhante ao padrão em pacientes com POAG. Em curvas de 24 horas, os pacientes com LTG e POAG tinham padrões mais pronunciados de foi à noite e à noite do que de manhã, com mais picos e maior flutuação de foi durante a noite do que durante a noite (7). Outros fatores podem corroborar a hipótese de uma tensão mecânica primária relacionada com a PIO em LTG, como a presença de mudanças nas vias de saída de humor aquoso semelhantes às que ocorrem em POAG (10).
em doentes em que o LTG pode ser considerado uma doença no espectro de POAG, devem ser implementadas estratégias diagnósticas e terapêuticas semelhantes às dos doentes com glaucoma hiperbárico, com a ajuda de um oftalmologista (figura).
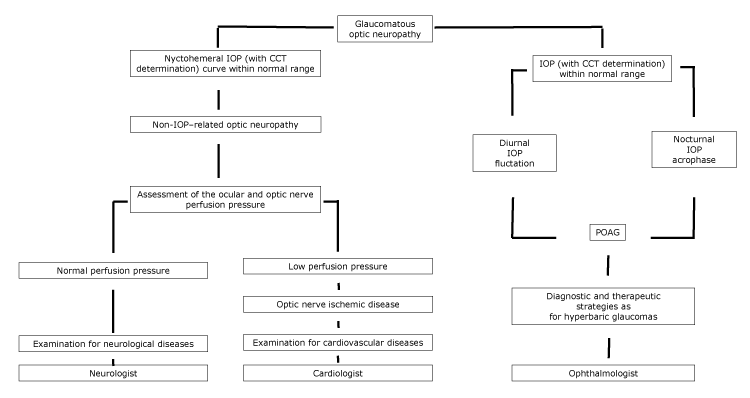
figura.
flowchart proposto de neuropatia óptica, com referência especializada, de acordo com as características da FOI nychthemeral. Abreviaturas: CCT, espessura central da córnea; IOP, pressão intra-ocular; POAG, glaucoma primário de ângulo aberto. a aparência do disco óptico é secundária à hipoperfusão do nervo óptico devido a doenças vasculares?
em doentes com curvas LTG e FOIINTEMERAL normais, os factores mecânicos não podem ser responsáveis pela neuropatia óptica; podem estar envolvidos factores independentes da pressão, sendo as alterações vasculares potencialmente as mais importantes (5). Pode observar-se neuropatia óptica de tipo glaucomatoso em doentes com história de ocorrência cardiovascular ou com aterosclerose crónica ou doenças arteriais obstrutivas (11). Em doentes com LTG (5) observou-se também uma velocidade reduzida do fluxo sanguíneo nas artérias retrobulbar e na circulação cerebral, uma baixa pressão arterial diastólica e um diâmetro menor do vaso central da retina. Nestes doentes, a patogénese da doença deve-se a uma pressão de perfusão ocular diminuída, principalmente ligada à desregulação vascular primária ou a uma disfunção generalizada do sistema nervoso endotelial ou autónomo (5,11). No entanto, não é claro se estes factores foram a causa ou o resultado da neuropatia óptica. De um ponto de vista clínico, o LTG mostra uma maior incidência de hemorragias no disco e é mais frequentemente associado a doenças vasculares como enxaqueca, apnéia obstrutiva do sono, ou síndrome de Raynaud do que com o IOP (5). Por último, cerca de metade dos doentes com GTTT com doença pré-perimétrica apresentam progressão danificada apesar dos valores normais da PIO (12). Todos estes achados sugerem o importante papel da desregulação vascular.em doentes com doenças cardiovasculares, a recaptação do disco óptico pode não progredir se a causa subjacente da neuropatia óptica tiver sido controlada. Além disso, os doentes com LTG podem apresentar atrofia circumpapilar, bem como microinfarcas corticais cerebrais, que são sinais de isquemia (5). Nos doentes em que as doenças vasculares induzem uma hipoperfusão do nervo óptico, deve ser realizado um diagnóstico completo das doenças cardiovasculares, com a ajuda de um cardiologista (figura).o LTG deve ser incluído num espectro de neuropatias ópticas congénitas e adquiridas que possam simular uma neuropatia óptica Glaucomatosa?quando foram excluídas as causas mais frequentes de recorte do disco óptico, deve ser considerada a possibilidade de neuropatia óptica neurodegenerativa. Estes casos são os mais frustrantes, porque os danos no disco óptico progridem mesmo após a PIO ter sido baixada. Muitas neuropatias ópticas congénitas e adquiridas estão incluídas neste grupo de casos, e a diferenciação entre o corte glaucomatoso e o nonglaucomatoso pode ser um desafio mesmo para observadores experientes (13). Entre as formas congênitas de corte de disco óptico, megalopapila, atrofia óptica autossômica dominante, e neuropatia óptica hereditária de Leber poderia produzir uma escavação de disco óptico simulando neuropatia óptica glaucomatosa.as neuropatias adquiridas podem ser secundárias a causas inflamatórias, compressivas, tóxicas e traumáticas. A neurite óptica pode produzir um aumento da razão copo-disco que, embora unilateral, pode ser confundida com neuropatia óptica glaucomatosa. Lesões compressivas incluindo meningioma, adenoma da pituitária, craniofaringioma, e aneurisma da artéria carótida interna podem levar a um recorte óptico assimétrico e erroneamente atribuído ao LTG. A intoxicação por metanol e etambutol pode produzir uma coloração bilateral do disco óptico semelhante à neuropatia óptica glaucomatosa, secundária à perda axonal. Assim, quando se observa uma Copa assimétrica ampliada, é necessária mais investigação neuro-oftalmológica (13).por último, entre as condições que levaram à recorte do disco óptico, o envelhecimento tem um papel principal. Harju et al descobriu que o grau de recorte de disco óptico aumentou em participantes saudáveis mais velhos do estudo por causa da perda de fibra fisiológica. Sua população de estudo foi apropriada e representou um conjunto de olhos saudáveis sem glaucoma; ao longo de 11 anos de acompanhamento, nenhum participante do estudo desenvolveu mudanças de campo visual, e nenhum aumento significativo na Pio foi registrado (14). Neste último caso, deve ser realizado um diagnóstico completo de doenças neurológicas, com a ajuda de um neurologista (figura).a descrição das características do disco óptico combinada com a imagem da camada de fibra nervosa da retina e a topografia do disco óptico permite a diferenciação entre a cobertura do disco óptico glaucomatoso e a cobertura do disco óptico nonglaucomatoso. Além disso, uma análise cuidadosa da história dos doentes, juntamente com a avaliação morfológica e funcional do nervo óptico, ajuda a identificar distúrbios.o termo LTG pode ser um oximoro, uma memória nostálgica do passado quando um diagnóstico definido não era possível. Usar o termo é como usar a palavra “febre” quando não há alta temperatura ou dizer festina lenta (“mais pressa, menos velocidade”). O termo LTG pode ser enganoso ou impreciso, porque se refere a um problema mecânico da PIO, enquanto que a redução do disco óptico e a perda do campo visual nos olhos com pressão intra-ocular normal são causadas por outros fatores. Portanto, na presença de corte de disco óptico com pio normal, os oftalmologistas devem investigar outras causas plausíveis de lesão do nervo óptico além da pressão intra-ocular.
Top
agradecimentos
Este estudo não recebeu nenhuma subvenção específica de qualquer agência de Financiamento nos setores público, comercial ou sem fins lucrativos.
Top
Informação do autor
autor correspondente: Luca Agnifili, MD, PhD, Ophthalmology Clinic, Via dei Vestini, 66100, Chieti (CH), Itália. Telefone: + 39-0871-358489. E-mail: [email protected] Autor afiliações: 1departição de Medicina e Ciências da Saúde, Universidade de Molise, Campobasso, Itália. 2Department of Medicine and Aging Science, Ophthalmology Clinic, University G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14-21. CrossRefexternal icon PubMed External icon
- De Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; Low-pressure Glaucoma Treatment Group. Factores de risco para a progressão do campo visual no estudo de tratamento de glaucoma de baixa pressão. Am J Ophthalmol 2012; 154 (4):702-11. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Cartwright MJ, Anderson Dr. Correlation of asymmetric damage with asymmetric intraocular pressure in normal-tension glaucoma (low-tension glaucoma). Arch Ophthalmol 1988; 106 (7):898-900. CrossRefexternal icon PubMedexternal icon
Top