zasadowość Amin i pKaH
określając ilościowo zasadowość Amin, używając „PKA sprzężonego kwasu”, vel „pKaH”
Jak zmierzyć zasadowość aminy? Przykład: jaka jest mocniejsza podstawa: pirydyna czy piperydyna?
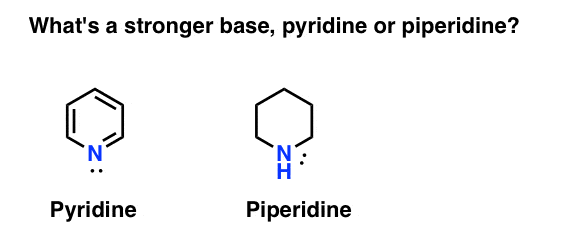
jeśli powiedziałeś piperydyna, gratulacje – to rzeczywiście jest silniejsza zasada.
ale dlaczego? A o ile silniejsza? Jak można próbować odpowiedzieć na te pytania? Po tym wszystkim, możemy łatwo porównać siłę kwasów, badając ich pKa. czy nie powinniśmy być w stanie zrobić to samo z zasadami?
tak, w pewnym sensie. Oto dwa kluczowe punkty na dziś:
- najlepszym sposobem na określenie zasadowości aminy jest zbadanie pKa jej sprzężonego kwasu.
- im wyższy pKa sprzężonego kwasu, tym silniejsza zasada.
w tym poście pokażemy kilka konkretnych przykładów użycia wartości pKa do porównania zasadowości Amin.
w kolejnym poście zbadamy kilka kluczowych trendów leżących u podstaw zasadowości Amin.
spis treści
- szybki przegląd: kwasy, zasady, kwasy sprzężone i zasady sprzężone
- używanie pKa do pomiaru kwasowości
- używanie PKA do kwantyfikacji zasadowości Amin
- „PKA kwasu sprzężonego” można skrócić do „pKaH”
- używanie pKaH do określania względnych zasad Amin
- niektóre słowa ostrzeżenia na temat zasad wartości PKA dla amin
- jakie kluczowe czynniki regulują zasadowość Amin?
- uwagi
1. Szybki Przegląd: Kwasy, zasady, kwasy sprzężone i zasady sprzężone
Po pierwsze, przyjrzyjmy się szybko podstawom zasadowości.
w każdej reakcji kwasowo-zasadowej występują cztery podmioty.
- baza jest gatunkiem, który przekazuje samotną parę do H+ (znanego również jako „proton” lub „jądro wodoru”). To tam, gdzie tworzy się nowe Wiązanie do H (np. pirydyna, poniżej)
- sprzężony kwas jest gatunkiem, który powoduje, że zasada tworzy wiązanie do H (np. „pirydinium” , który ma nowe Wiązanie N–H)
- kwas jest gatunkiem, który traci H+ . To tam pęka Wiązanie do H (np. H-Cl)
- sprzężona zasada to gatunek, który pozostaje po tym, jak kwas przekazuje h+ do zasady (np. Cl-)
tutaj pirydyna i piperydyna w działaniu. Podążając za tworzącymi się i pękającymi więzami, możesz zidentyfikować każdego aktora.
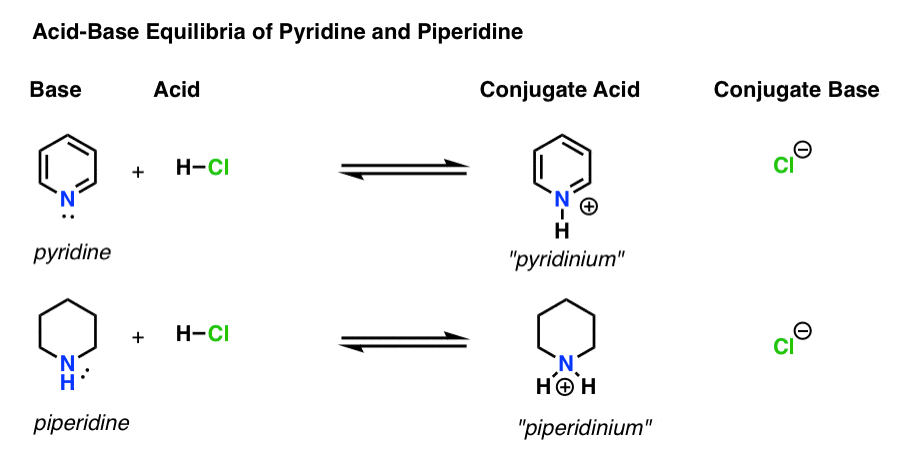
2. Używając pKa do pomiaru kwasowości
każda reakcja kwasowo-zasadowa może być zapisana jako równowaga między reakcją do przodu i do tyłu. Widzieliśmy, że stała kwasowości, Ka, jest miarą tego, jak łatwo gatunek dysocjuje, dając h+ i sprzężoną zasadę.
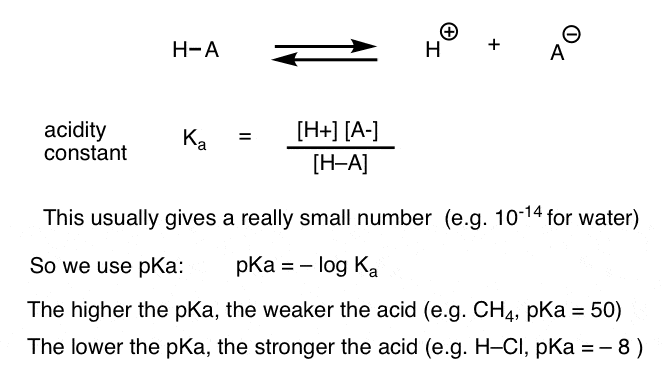
dla wygody używamy ujemnego logarytmu Ka, zwanego pKa, który jest podobny do znanej skali pH, ale może wykraczać poza 14, ponieważ nie jest ściśle ograniczony do wodnego rozpuszczalnika. wartości pKa wahają się od -10 lub więcej dla bardzo silnych kwasów (np. kwas hydroiodowy, H–I) do 50 i więcej dla niektórych węglowodorów (np. etan).
Jak możemy zastosować te pojęcia do pomiaru zasadowości? Czy nie moglibyśmy zmienić rzeczy i zdefiniować pojęcia, Kb, które jest równowagą dla tego, jak łatwo gatunek łączy się z H+, zdefiniować pKb jako jego ujemny log i porównać bazy, patrząc na ich wartości pKb?
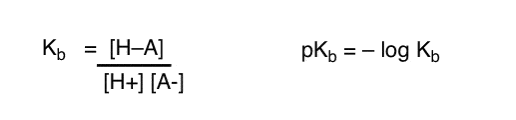
tak…. moglibyśmy. Chyba tak. Gdybyśmy musieli. Generalnie jednak opinia chemików organicznych na ten temat jest „wkręcona”.
w końcu wartości pKa zostały zmierzone dla tysięcy cząsteczek organicznych. Czy ktoś naprawdę chce pamiętać o ogromnym zestawie wartości pKb? Nie ma mowy!
zamiast tego możemy łatwo użyć wartości pKa jako pośredniego pomiaru zasadowości. Oto jak.
3. Używając wartości pKa do ilościowego określenia zasadowości Amin
przypomnij sobie te dwie nieśmiertelne linie prozy, które warto recytować sobie co noc:
- im silniejszy kwas, tym słabsza sprzężona zasada.
- im słabszy kwas, tym silniejsza sprzężona zasada.
zmierzono pKa dla sprzężonego kwasu pirydyny („pirydynium”). Około 5,2 .
mamy również wartość pKa dla sprzężonego kwasu piperydyny. Jest około 11 .
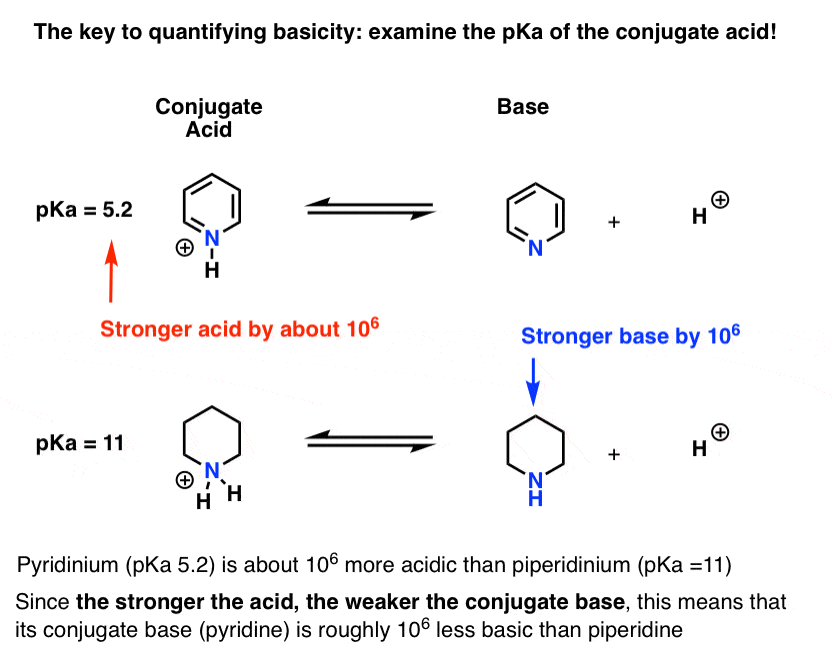
z tych wartości PKA możemy powiedzieć, że sprzężony kwas pirydyny jest silniejszy niż sprzężony kwas piperydyny o około 6 jednostek pKa. Ponieważ każda jednostka pKa reprezentuje współczynnik 10, jest to współczynnik około 1 miliona.
ponieważ „im silniejszy kwas, tym słabsza sprzężona zasada”, pirydyna jest zatem słabszą zasadą niż piperydyna o współczynnik 1 miliona.
4. „PKa sprzężonego kwasu „można skrócić do”pKaH „
termin” PKA sprzężonego kwasu ” jest nieco przydatny do regularnego używania. Będąc naturalnie leniwymi, chcielibyśmy to nieco skondensować do powszechnego użytku.
ponieważ sprzężony kwas Zasady („B”) to” BH”, możemy skrócić” pKa sprzężonego kwasu zasady ” jako jego pKaH.
To pozwala nam powiedzieć, że pKaH pirydyny wynosi 5,2, a pKaH piperydyny wynosi 11.
następnie możemy zagłębić się w literaturę, aby znaleźć inne bazy, z którymi można ją porównać.
na przykład, jak podstawowy jest amoniak (NH3) ? Sprzężony kwas amoniaku, NH4 (+), wynosi 9,2 . Równoważnie, możemy powiedzieć, że pKaH amoniaku wynosi 9,2. To stawia go pomiędzy pirydyną i piperydyną w skali zasadowości.
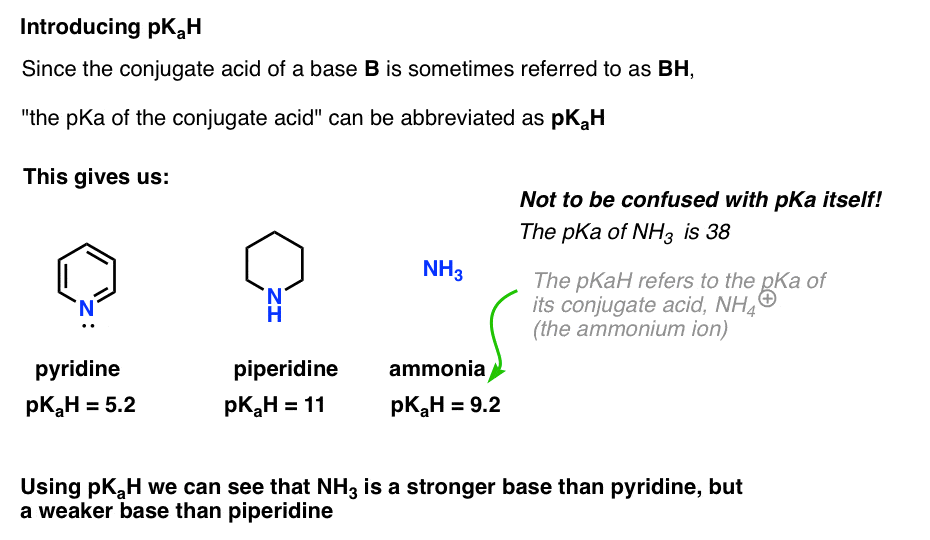
należy pamiętać, że bardzo ważne jest, aby nie mylić pKaH z pKa. PKaH amoniaku wynosi 9,2, co oznacza kwasowość jego sprzężonego kwasu, NH4 (+).
pKa samego amoniaku wynosi 38, co oznacza stałą równowagi dla dysocjacji NH3, dając jej sprzężoną zasadę, NH2 ( -) I H+.
oznacza to, że 38 jest pKaH jonu amidowego NH2 (–), który można było spotkać wcześniej jako mocną zasadę (NaNH2) używaną do deprotonacji końcowych alkinów (pKa =25). Używając pKaH, możemy określić, że NH2 ( – ) jest około (38-9) = 29 rzędów wielkości bardziej podstawowe niż NH3 !
5. Używanie pKaH do określania względnych zasad Amin
używanie pKaH do określania względnych mocy zasad jest całkiem użyteczną sztuczką.
oto kilka reprezentatywnych przykładów cząsteczek zawierających azot. Poniżej znajduje się pKa ich sprzężonych kwasów.
jaka jest tu najsilniejsza baza? Co jest najsłabsze?
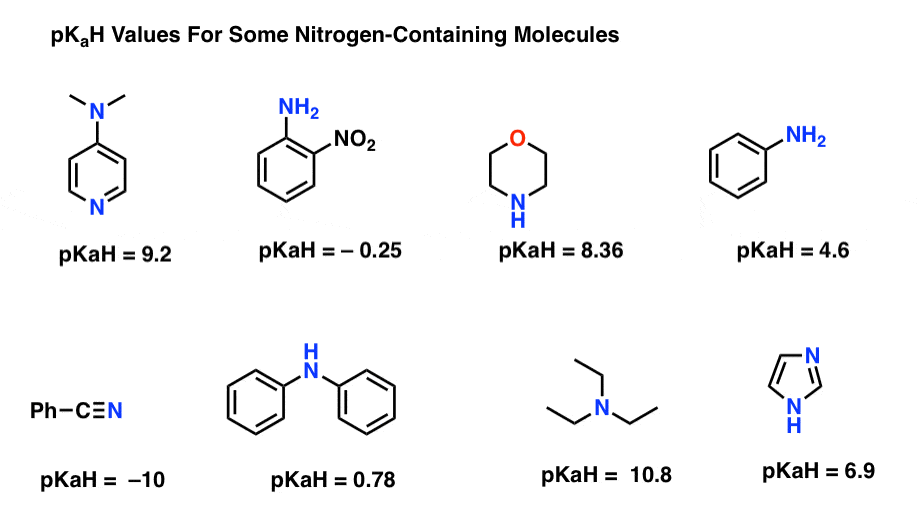
najniższa wartość pKaH wynosi tutaj -10 dla nitrylu (lewy dolny róg). Oznacza to, że nitryl jest najmniej zasadowy ze wszystkich tych cząsteczek.
najwyższa wartość pKaH wynosi tutaj 10,8 dla trietyloaminy. To sprawia, że trietyloamina jest najsilniejszą bazą spośród wszystkich wymienionych.
kilka słów ostrożności na temat wartości PKA dla Amin
dwie rzeczy, na które należy zwrócić uwagę, szczególnie podczas czytania innych źródeł online na ten temat.
Po pierwsze, Czasami wartości pKaH dla Amin są podawane jako wartości pKa , bez wyjaśnienia. Najlepsze stoły pKa tego nie zrobią, ale trudno jest sortować pszenicę z plew, gdy dopiero zaczynasz.
Jeśli widzisz anomalnie niską wartość pKa dla aminy, prawdopodobnie odnosi się to do pKaH sprzężonego kwasu.
na przykład, oto tabela pKa, w której PKA metyloaminy (CH3NH2) jest wymieniony jako 10,63.
to mało. Mam nadzieję, że w tym momencie taka wartość 10 dla PKA aminy powinna wydawać się dziwna, zwłaszcza, że pKa blisko spokrewnionego NH3 wynosi 38.
wartość 10,63 w rzeczywistości odnosi się do PKA sprzężonego kwasu metyloaminy, a nie samej metyloaminy. To wartość pKaH.
podobnie, w tej samej tabeli wymieniono trimetyloaminę jako mającą pKa 9,8 . Ponownie, to jest rzeczywiście jego pKaH. Nie mogę znaleźć rzeczywistej wartości PKA dla trimetyloaminy, ale domyślam się, że jest to >40, ponieważ sprzężona zasada trimetyloaminy to karbanion (CH3)2N–CH2(–) ).
drugim, mniej powszechnym źródłem nieporozumień jest to, że czasami pKaH aminy jest zgłaszany jako jej pKb, na przykład w tej tabeli, która podaje pKb NH3 jako 9.2 . Jest to niedokładne.
znowu wartości pKb w chemii organicznej nie wychodzą zbyt często, chociaż podobno czasami pojawiają się na DAT/MCAT.
7. Jakie Kluczowe Czynniki Regulują Zasadowość Amin?
teraz, gdy nauczyliśmy się przynajmniej jak ilościowo i interpretować wartości pKa amin i ich sprzężonych kwasów, możemy zacząć zadawać kluczowe pytanie: dlaczego? Jakie kluczowe czynniki regulują zasadowość Amin? Jakie są ważne trendy?
na przykład dlaczego pirydyna jest słabszą zasadą niż piperydyna? Dlaczego nitryle są jeszcze słabsze Zasady? Dlaczego grupy wycofujące elektrony mają tendencję do osłabienia zasad Amin?
dobra wiadomość jest taka, że jeśli już rozumiesz czynniki, które rządzą kwasowością, po prostu musisz zastosować dokładnie te same zasady-ale odwrotnie!
omówimy to w następnym poście. Pięć czynników wpływających na zasadowość Amin
uwagi
przypis 1. Istnieje wiele kwasów, które nie są zasadami (np. NH4, w którym brakuje samotnej pary) i wiele zasad, które nie są kwasami, takich jak Cl (-), który nie jest w stanie zaakceptować samotnej pary. Dlatego powiedzenie „im silniejszy kwas, tym słabsza zasada” jest błędne.
przypis 2. Jest to pomiar uzyskany przy użyciu wody jako rozpuszczalnika. Można zobaczyć inną wartość, 3.4, która jest uzyskiwana, gdy dimetylosulfotlenek (DMSO) jest używany jako rozpuszczalnik. Zobacz tabele Bordwell pKa (DMSO)