Harvard Gazette
Joshi obecnie jest głównym członkiem wydziału Instytutu Wyss i profesorem nadzwyczajnym w Harvard ’ s Paulson School of Engineering and Applied Sciences (SEAS), a wkrótce zostanie mianowany profesorem na Northeastern University w Bostonie.
w poprzednich pracach Grupa Joshi wykazała, że samo-regenerujące się hydrożele bakteryjne mocno przymocowane do powierzchni śluzówki ex vivo, a po podaniu doustnym myszom wytrzymały surowe pH i warunki trawienne żołądka i jelita cienkiego bez wpływu na zdrowie zwierząt. Aby je wyprodukować, jego zespół zaprogramował laboratoryjny szczep E. coli do syntezy i wydzielania zmodyfikowanego białka CsgA, które jako część systemu „curli” E. coli montuje się w długie nanowłókna na zewnętrznej powierzchni bakterii. „Aby umożliwić adhezję śluzu, połączyliśmy CsgA z domeną wiążącą śluz różnych ludzkich czynników trefoil (TFFs), białek, które występują naturalnie w błonie śluzowej jelit i wiążą się z mucynami, głównymi białkami śluzowymi tam obecnymi. Wydzielane białka fuzyjne tworzą siatkę magazynującą wodę o przestrajalnych właściwościach hydrożelu”, powiedziała współautorka Anna Duraj-Thatte, doktorantka pracująca z Joshi. „Okazało się to prostą i solidną strategią produkcji samoodnawiających się materiałów mukoadhezyjnych o długim czasie przebywania w przewodzie pokarmowym myszy.”
powiązane

połączenie IBD–gut bug
nowe odkrycia ujawniają, jak choroba zapalna jelit zaburza mikrobiom
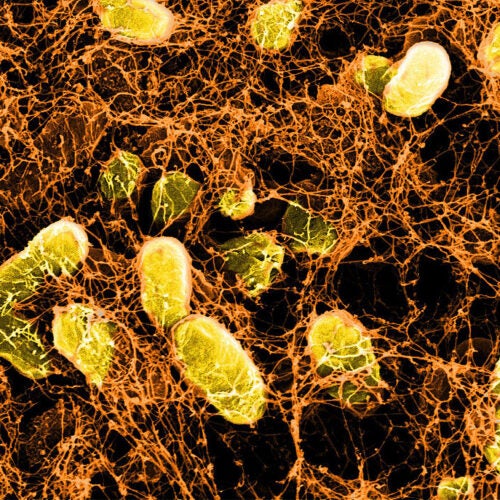
hydrożele probiotyczne leczą rany jelit, do których inne metody leczenia nie mogą dotrzeć
mogą otworzyć drzwi do nowych bioaktywnych strategii leczenia
w swoim nowym badaniu zespół dalej opierał się na tych odkryciach, wprowadzając urządzenie do produkcji jednego z hydrożeli mukoadhezyjnych opartych na TFF3 do szczepu nissle E. coli, który jest normalna bakteria jelitowa, która może rozwijać się w odcinkach jelita grubego i jelita ślepego przewodu pokarmowego dotkniętych IBD i jest obecnie sprzedawana w wielu komercyjnych preparatach probiotycznych. „Odkryliśmy, że nowo zaprojektowane bakterie Nissle, po podaniu doustnym, również zaludniły i przebywały w przewodzie pokarmowym, a ich włókna curli zintegrowane z warstwą śluzu jelitowego”, powiedział pierwszy autor Pichet Praveschotinunt, który jest studentem pod kierunkiem Joshi.
” Kiedy wywołaliśmy zapalenie okrężnicy w okrężnicach myszy, podając doustnie chemiczny siarczan sodu dekstranu, zwierzęta, które otrzymały e-plaster generujący. szczep coli nissle przez codzienne podawanie doodbytnicze, począwszy od trzech dni przed leczeniem chemicznym, miał znacznie szybsze gojenie i mniejszą reakcję zapalną, co spowodowało, że traciły znacznie mniejszą wagę i szybciej regenerowały się w porównaniu do zwierząt kontrolnych”, powiedział Praveschotinunt. „Ich nabłonek jelita grubego wykazywał bardziej normalną morfologię i mniejszą liczbę nacierających komórek odpornościowych.”
Joshi i jego zespół uważają, że ich podejście można opracować jako terapię towarzyszącą istniejącym terapiom przeciwzapalnym, immuno-tłumiącym i antybiotykowym, aby zminimalizować ekspozycję pacjentów na leki i potencjalnie zapewnić ochronę przed nawrotami IBD.
dodatkowymi autorami badania są badacze Instytutu Wyss Ilia Gelfat, Franziska Bahl i David B. Chou.
badanie było wspierane przez grant z National Institutes of Health, fundusze z Harvard ’ s Wyss Institute for biologically Inspired Engineering i Blavatnik Biomedical Accelerator oraz stypendium royal Thai government scholarship.
The Daily Gazette
Zapisz się na codzienne maile, aby otrzymywać najnowsze wiadomości.