Svak I Knærne: Miller Fisher Syndrom
Miller Fisher syndrom (MFS), en sjelden, selvbegrensende variant Av Guillain-Barré syndrom (GBS), er et anti-GQ1bIgG antistoffsyndrom som påvirker det perifere og sentrale nervesystemet.1 akutt neuromuskulær polyneuropatisk tilstand, MFS fører til en stigende lammelse med en klassisk presentasjonstriade av oftalmoplegi, ataksi og arefleksi. Forskere beskrev først den kliniske triaden i 1932.1 To tiår senere var Den Kanadiske slagspesialisten Charles Miller Fisher den første som publiserte en rapport i 1956 som beskrev de kliniske funnene og definerte tilstanden som en begrenset FORM FOR GBS.2
Symptomer oppstår over flere dager, ofte om vinteren og våren, vanligvis etter en virusinfeksjon, og pasienter opplever ofte diplopi som et av de første symptomene. Når en pasient presenterer symptomer som intermitterende esotropi, svekket horisontal sysler og faste mydriatiske elever, og din nevrologiske eksamen er unormal, er DET på tide å tenke PÅ GBS, spesielt MFS. Følgende tilfelle illustrerer relevante tegn og symptomer og gjenspeiler det typiske utfallet.
Historie
en 27 år Gammel Kaukasisk mann presentert FOR VA Eye Clinic i løpet av vårmånedene rapportering akutt innsettende kikkert dobbeltsyn som startet en dag før. Pasienten uttalte at det var konstant, men bare forekom ved avstandsvisning med objekter forskjøvet horisontalt. Det var ingen øye smerte eller sløret syn forbundet med diplopien. Han klaget også over nylig svimmelhet og balansevansker. Han rapporterte en sinusinfeksjon med betydelig paranasal overbelastning som startet en uke før dobbeltsynet. Tidligere okulære og medisinske historier var unremarkable; pasienten tok for øyeblikket ikke medisiner og hadde ingen medisinallergi.
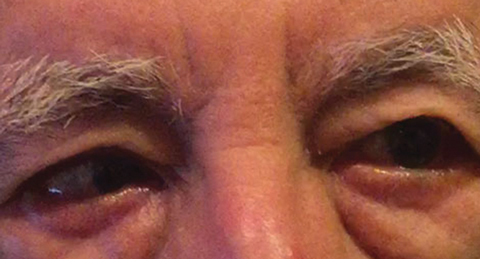
Fig. 1. Differensialdiagnosen etter baseline-undersøkelse inkluderte en delvis høyre CN VI parese, som kunne indikere en vaskulær tilstand, sett her hos en annen pasient. Klikk på bildet for å forstørre. Foto: Michael DelGiodice,OD
Diagnostiske Data
ved baseline undersøkelse var ukorrigerte visuelle acuiteter 20/20 – 2 OD og 20/25-2 OS. Pupillene var 5 mm like runde og reaktive mot lys uten afferent pupilldefekt. Extraocular motilities var fulle, glatte og nøyaktige i begge øynene uten begrensninger. Dekktest på avstand avslørte en intermittent fire til seks prisme diopter høyre esotropi i primær blikk som forekommer omtrent 50% av tiden. Utføre dekke test på nær avslørte en fire prisme diopter esophoria i primære blikk uten tropia.
selv om det ikke er gjennomført i dette tilfellet, bør klinikere dekke test i primær, høyre og venstre blikk. Hos pasienter med dobbeltsyn, vil cranial nerve six (CN VI) parese manifestere seg som ikke-comitant avvik, verre i høyre eller venstre blikk, avhengig av hvilken side parese er på. En dekompenserende phoria vil derimot vise comitant avvik. Refraktiv feil var -0,50 d sfære OD og -0,75 D sfære OS og visjonen ble korrigert til 20/20 i hvert øye. Intraokulært trykk var innenfor normale grenser i begge øynene. Anterior og posterior segment funn var unremarkable i høyre og venstre øyne. De optiske nerver virket sunne med et kopp-til-disk-forhold på 0,15 i begge øynene.
Differensialdiagnoser inkluderte delvis høyre CN VI parese (Figur 1), myasthenia gravis, en kompresjonsprosess og en dekompenserende avstandsesophoria som forårsaket intermitterende høyre esotropi. Pasienten nektet enhver tidligere historie med binokulær diplopi.Avbildning av hjernen og baner ble bestilt av eye clinic for å utelukke hjerneinvolvering, inkludert en komprimerende lesjon. Computertomografi (CT) skanninger av hjernen og baner ble utført og tolket av personalet neuroradiologist. CT ble valgt i stedet for magnetisk resonans imaging (MRI) på grunn av timing og tilgjengelighet; testing og resultater kunne oppnås samme DAG MED CT i klinikken etter timer. Resultatene var unremarkable uten tegn på intrakranial blødning, kompressiv lesjon eller akutt infarkt.
CT av paranasale bihuler viste moderat til alvorlig kronisk paranasal sinus sykdom og fullstendig opacifisering av høyre maksillary sinus. Det var ingen forlengelse i bane. Pasientens familielege ble informert om pasientens symptomer, funn av øyeeksamen og CT – bilderesultater og startet behandling for maksillær bihulebetennelse med en oral azitromycin fem-dagers dosepakke og instruerte pasienten om å følge opp med øyeklinikken.pasienten kom tilbake fem dager senere etter å ha fullført sitt orale azitromycin-kurs og uttalte at han ikke opplevde noen forbedring i avstandsdiplopien; i tillegg opplevde han utbruddet av betydelig fotofobi og periokulær smerte rundt begge øynene. Pasienten uttalte at hans gangforstyrrelser og gangproblemer også ble forverret. Ved undersøkelse forblir best korrigerte visuelle acuities 20/20 i høyre og venstre øyne. Pupillene ble utvidet med 8,5 mm uten reaktivitet for lys i begge øynene (Figur 2). Ekstraokulære motiliteter viste lateral begrensning med smerte ved bevegelse i høyre øye og medial begrensning med smerte ved bevegelse i venstre øye i samsvar med en høyre blikk parese (Figur 3). Horisontale og vertikale sysler var saccadiske med unøyaktige og rykkete bevegelser. Anterior og posterior segment funn forble unremarkable OU.Differensialdiagnoser etter oftalmologisk undersøkelse inkluderte venstre internukleær oftalmoplegi, høyre gaze parese og høyre gaze parese med venstre internukleær oftalmoplegi, noe som kunne forklare ekstraokulære motilitetsfunn. Andre differensialer inkluderer en midbrain lesjon eller myasthenia gravis. Differensialdiagnoser for pupil dilatasjon inkluderer tredje nerve (CN III) parese, traumer og farmakologisk dilatasjon. Pasienten hadde ingen andre funn i samsvar med en tredje nerveparese og nektet traumer eller eksponering for farmakologiske midler.
pasienten ble henvist til nevrologi for videre vurdering. Nevrologisk undersøkelse rapporterte at pasienten var helt våken og orientert uten tap av ansiktsfølelse. Pasienten viste mild ataksi med vanskeligheter med å gå i tandem og stå fra en hekkeposisjon. Proksimal svakhet i både øvre og nedre ekstremiteter og unormale reflekser var tilstede. Alle sensoriske modaliteter var intakte. MR og magnetisk resonans angiografi (mra) i hjernen og baner var unremarkable. Cerebrospinalvæskeprotein ble forhøyet ved 75 mg / dL (referanseområde: 15 mg/dl til 45 mg / dL) uten andre abnormiteter. Electromyogram testing var unremarkable og viste ingen abnormiteter i nervedannelse fra ryggraden til føttene og hendene.
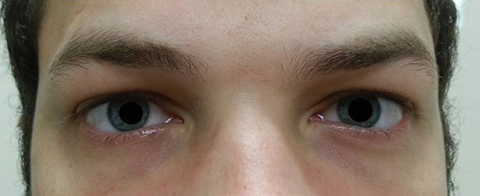
Fig. 2. Pasientens pupiller ble utvidet 8,5 mm uten reaktivitet i høyre eller venstre øye. Klikk på bildet for å forstørre.
Diagnose
pasienten presenterte akutte symptomer på diplopi, ataksi og arefleksi. Gitt intermitterende rett esotropi, svekket horisontal sysler, fast mydriatisk pupil, mild ataksi og unormale reflekser på nevrologisk undersøkelse og forhøyet cerebrospinalvæskeprotein, ble diagnosen MFS gjort. Pasienten ble innlagt på sykehuset for å overvåke for ytterligere komplikasjoner. En øyelapp ble gitt til pasienten for å dekke høyre øye etter behov for diplopi.
Ingen publiserte diagnostiske kriterier for Miller Fisher syndrom eksisterer for øyeblikket. Diagnosen gjøres vanligvis gjennom presentasjon av den kliniske triaden sammen med bildebehandling og cerebrospinalvæskestudier. MR er vanligvis unremarkable i tilstanden, selv om enkelte studier har vist sentrale lesjoner i midbrain, pons og nedre medulla. Elektrofysiologiske studier viser redusert eller unormal perifer sensorisk ledning.17
Cerebrospinalvæskeprotein er ofte forhøyet uten andre unormale funn. I en landemerkestudie viste 64,4% av mfs-pasientene forhøyet spinalvæskeprotein.8 en positiv Anti-GQ1b IgG antistofftest muliggjør en endelig diagnose. I en studie var anti-GQ1b IgG antistoff tilstede hos opptil 95% av pasientene med tilstanden og fraværende i kontroller.3
nevrologen diagnostiserte pasienten MED MFS basert på den kliniske triaden av oftalmoplegi, ataksi og arefleksi, en unremarkable MR og mra i hjernen og forhøyet cerebrospinalvæskeprotein. Derfor ble ikke anti-GQ1b IgG antistofftesting utført i dette tilfellet.
Flere kliniske trekk ved MFS er også sett I Guillain-Barré syndrom og Bickerstaff hjernestammen encefalitt, noe som gjør diagnosen utfordrende. Pasienter med Bare Guillain-Barrinois tilstede med svakhet i lemmer, sensorisk tap, kranialnevropati og arefleksi uten oftalmologiske manifestasjoner. Pasienter med Bickerstaff hjernestammen encefalitt vanligvis tilstede med oftalmoplegi, ataksi, hyper-refleksia og en forstyrret bevissthet. Siden flere symptomer og tegn er til stede i alle tre forhold, er anti-GQ1b IgG antistoff titer testing nyttig for en mer definitiv diagnose. Anti-GQ1b IgG-antistoff er positivt hos Et stort flertall Av Miller Fisher syndrom-pasienter sammenlignet med 66% hos Bickerstaffs hjernestamme encefalitt og 26% hos Guillain-Barré syndrom-pasienter.16
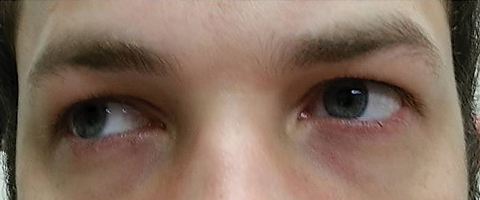
Fig. 3. Extraocular motilities avslørte begrensning i dextroversion. Klikk på bildet for å forstørre.
Behandling og Oppfølging
pasienten ble evaluert dagen etter opptak, da han uttalte at han ikke opplevde noen visuelle endringer eller forbedring i balanse. Binokulær diplopi var fortsatt konstant; derfor forblir det høyre øyet lappet. Øyesmerter med langt blikk og raske øyebevegelser var fortsatt tilstede. På begrenset sengen undersøkelse, best korrigert synshemmede forble 20/20 i høyre og venstre øyne. Elevene ble utvidet ved 8.0mm i begge øyne med minimal reaktivitet, noe som ble litt forbedret fra dagen før. Fargesynet var normalt i høyre og venstre øyne. Extraocular motilities var fulle i alle kvadranter med smerte fortsatt tilstede på langt horisontale blikk. Horisontale sysler forble saccadic med jerky bevegelser og endepunkt nystagmus. De optiske nerver virket sunne med forskjellige marginer og et kopp til diskforhold på 0, 15 i begge øynene.To dager etter uttalte pasienten en forbedring i alle symptomer og at øynene hans «føler seg bedre i dag enn de har vært på en stund.»Øye smerte og kikkert diplopi ble begge løst . Visuelle akuiteter forblir 20/20 i høyre og venstre øyne. Elevstørrelser var 7,5 mm i mørke og 7,0 mm i lys med forbedret direkte og samtykkende respons i begge øyne. Extraocular motilities var fulle i alle kvadranter uten øye smerte. Horisontale sysler forble saccadic med jerky bevegelser og endepunkt nystagmus. Neurologisk undersøkelse viste unormale reflekser, som holdt seg stabile. Behandlingsalternativene for MFS inkluderer plasmaferese og intravenøs (IV) immunglobulin IgG, men disse ble holdt tilbake gitt forbedring i oftalmoplegi og ataksi.Fire dager Senere rapporterte pasienten at alle symptomene fortsatt var bedre, med noen problemer med å fokusere og spore mens du bruker datamaskinen. Balansen var 80% løst og det var få forekomster av avstandsdiplopi. Acuities forble 20/20 OU. Elevene var 5,5 mm i mørke og 4,0 mm i lys med 3 + direkte og samtykkende svar OU. Extraocular motilities var fulle i alle kvadranter uten øye smerte. Horisontale sysler ble forbedret, uten saccadic bevegelser. Monokulær innkvartering var normal, som ble målt henholdsvis 8,5 og 9 prisme dioptre OD og OS.En uke senere rapporterte pasienten at hans syn kom tilbake til nesten normalt uten diplopi og milde problemer med fokusering og sporing. Balansen ble 100% løst. Visuelle akuiteter forblir 20/20 i høyre og venstre øyne. Elevstørrelser var 5,5 mm i mørke, 4,0 mm i lys med 4 + direkte og samtykkende svar OU. Extraocular motilities var fulle i alle kvadranter uten øye smerte. Horisontale sysler forbedret uten observerte saccadic bevegelser. Okulær helse var unremarkable OU.
Behandling ble holdt tilbake gitt oppløsning av oftalmoplegi og ataksi med stabil arefleksi. Full gjenoppretting av ophthalmoplegi og ataksi tok to uker. Ledelsen inkluderte tett oppfølging og oppfølging i fire uker; pasienten ble rådet til å returnere tidligere hvis noen av hans symptomer returnerte.
Kliniske Trekk
i godt beskrevne studier av MFS presenterte alle pasienter den kliniske triaden av oftalmoplegi, ataksi og arefleksi.4,5 Symptomdebut oppstår vanligvis over flere dager, og pasienter lider av en virusinfeksjon en til fire uker før utbruddet av kliniske symptomer.4,5 ifølge en studie av 50 pasienter med tilstanden er gjennomsnittlig intervall mellom infeksjonsutbrudd og utvikling av nevrologiske symptomer åtte dager.4 andre tegn på MFS inkluderer sløret tale, vanskeligheter med å svelge og et unormalt ansiktsuttrykk med manglende evne til å smile eller fløyte.
Oftalmologiske egenskaper. Utøvere bør være på utkikk etter mydriasis, lokk tilbaketrekning, akutt vinkel lukning og diplopi sekundært til nervepalsier som påvirker CN III, IV OG VI. 3,8,10,22,24 Diplopi er det vanligste oftalmologiske symptomet rapportert i MANGE mfs-studier.8,16,25,26,27 Dobbeltsyn er også det første symptomet rapportert hos 38,6% av 223 pasienter i en landemerkestudie og 65% av 466 pasienter i en andre studie.8,27 i den andre studien viste 100% av pasientene ekstern oftalmoplegi, mens intern oftalmoplegi var tilstede hos 35% av pasientene.27 Ekstern oftalmoplegi refererer til forringelse av eksterne ekstraokulære muskler. Intern oftalmoplegi refererer til nedsatt pupillær sphincter og ciliary muskel. Komplett oftalmoplegi påvirker både eksterne og indre muskler.
i en retrospektiv studie av 19 pasienter med MFS, alle presentert med en eller flere nerve palsies påvirker extraocular muskler.25 andre studier viser AT MFS-pasienter kan oppleve flere kranialnervepalsies, som kan manifestere bilateralt.22,24,25 en vanlig funn funnet blant anti-GQ1b IgG positive lidelser er bortføring underskudd forenlig med en ensidig ELLER bilateral CN VI parese.26,28 intern oftalmoplegi forårsaker pupil mydriasis, hvor pupilkonstruksjon til lys og / eller nær stimulering kan variere fra minimal til fraværende.8,26 i en rapport var mydriasis tilstede hos 42% av pasientene. Involvering av CN VII forekom hos ca. 45,7% av MFS-pasientene som forårsaket ansiktssvakhet, manglende evne til å smile eller plystre.8
Ataksi. Årsaken til denne kliniske funksjonen ved MFS er ikke fullt ut forstått. Debatt eksisterer om ataksi er forårsaket av dysfunksjon sentralt i cerebellum eller perifert. Den første hypotesen, foreslått Av Dr. Fisher, postulerte involvering av Ia-afferente nevroner.2 Dette ble støttet av en andre studie tiår senere, som viste abnormiteter av Ia-afferente fibre I MFS.11 Unormal perifer nerve involvering har også blitt foreslått med en mismatch mellom proprioceptive input fra muskel spindler og kinestetisk informasjon fra felles reseptorer.12
det har også vært støttende bevis på at ataksi stammer fra cerebellum. En overvekt av Anti-GQ1b IgG-antistoff i cerebellum ble funnet ved bruk av immunocytokjemisk farging av humant cerebellum og ytterligere bekreftet med western blot-studier, som viste økt anti-GQ1b IgG-antistoff hos MFS-pasienter sammenlignet med kontroll, selv om mekanismen for cerebellar involvering ikke er studert.13,14 i 2015 publiserte forskere en saksrapport om EN MFS-pasient som gjennomgikk MR. Det var redusert N-acetylaspartat / kreatinforhold, noe som tyder på cerebellar dysfunksjon, som gikk tilbake til normal 2,5 måneder etter utvinning.23
Arefleksi. Denne kliniske funksjonen, sammen med depresjon av dype senereflekser, er et tegn på perifert nervesystemaffeksjon i MFS. Elektrofysiologiske studier har validert unormal perifer nervedannelse i GBS og MFS.3 i en studie ble 81,6% av MFS-tilfellene presentert med arefexia.8 En annen landemerkestudie viste at alle pasienter opplevde arefleksi, som fortsatt var tilstede seks måneder etter utbruddet.4
Hvor Vanlig ER MFS?
Epidemiologiske data om Miller Fisher syndrom er begrenset. Forekomsten AV MFS er ganske sjelden, forekommer i 0,09 per 100 000 mennesker årlig.3 MFS forekommer vanligere hos pasienter Med Guillain-Barré syndrom, fra 3% til 25%.4,6,7 denne foreningen forekommer mer hos pasienter Med Fjernøsten nedstigning, noe som tyder på en mulig genetisk komponent TIL MFS. Gjennomsnittlig alder for utbruddet er 43, med en rekkevidde på 13 til 78,5 MFS påvirker menn dobbelt så mye som kvinner med et forhold på to til 1,03,5 MFS forekommer mer i vinter-og vårsesongene.5,6,8 den eksakte årsaken til sesongens predileksjon er ikke fastslått, men er sannsynligvis forbundet med tilstandens postinfeksjonelle natur, da bakterielle og virale infeksjoner har vist seg å utløse en autoimmun respons som forårsaker produksjon av Anti-GQ1b IgG-antistoffet i MFS.
Patofysiologi
Patofysiologien Til Miller Fisher syndrom er ikke godt forstått; imidlertid finnes det flere hypoteser fra immunologiske og histologiske studier. Det er velkjent at tilstanden ligger innenfor spekteret av anti-GQ1b IgG antistoff syndromer sammen Med Guillain-Barré syndrom og Bickerstaff hjernestammen encefalitt.
gangliosid GQ1b er en gruppe komplekse lipider involvert i sentrale og perifere nervesystemer. GQ1b er en komponent i plasmamembranstrukturen i kranialnervene som leverer de ekstraokulære musklene og er involvert i cellefunksjon ved det presynaptiske nevromuskulære krysset.
en autoimmun mekanisme fra en foregående utløsende infeksjon vil produsere anti-GQ1b IgG antistoff, som skader gangliosid GQ1b funksjon, forårsaker demyelinering. Histologiske studier har vist demyelinisering og aksonal hevelse i perifere og oculomotoriske kraniale nerver.15 anti-GQ1bIgG-antistoffet er fraværende hos friske pasienter, men positivt hos over 90% av pasientene med MFS.16,25
Bakterielle og virale infeksjoner har vist seg å utløse en autoimmun respons, forårsaker produksjon av anti-GQ 1b IgG antistoff. Følgende smittestoffer som har vært assosiert med MFS inkluderer mycoplasma pneumoni, HIV, Campylobacter jejuni, Hemophilus influensa, Helicobacter pylori og Epstein-Barr virus.4,16 i en rapport som så på 466 mfs-pasienter, hadde 90% en antecedent sykdom, inkludert øvre luftveisinfeksjon, diare eller begge deler.27
Prognose og Behandling
Miller Fisher syndrom er en selvbegrensende sykdom og har en samlet positiv prognose. Symptomene generelt bedre etter noen uker med full gjenoppretting vanligvis oppstår i to til tre måneder. I en studie startet bedring med en median på 13 dager fra symptomdebut, og fullstendig oppløsning av oftalmoplegi og ataksi forekom i løpet av seks måneder.4,5 Tilbakefall har blitt funnet å forekomme i mindre enn 3% av tilfellene.4,5
selv OM MFS vanligvis er selvbegrensende, har systemiske komplikasjoner vært forbundet med tilstanden. Øvre luftveisinfeksjoner er funnet hos 56% til 76% AV MFS-pasientene, som kan utvikle seg til respirasjonssvikt som krever mekanisk ventilasjon.4,18,19 andre sjeldne alvorlige komplikasjoner inkluderer kardiomyopati, laktacidose og koma.3,20
behandlingsalternativene for MFS inkluderer plasmaferese, iv immunglobulin IgG og monitorering uten behandling. Forskere postulerer at plasmaferese OG IV IgG kan være effektive for å øke oppløsningstiden siden antistoff Gq1b Er IgG i klassen og halveringstiden Til IgG er omtrent 21 dager, som er lengre enn De fem til seks dagers halveringstidene Til IgM og Iga.19 det er imidlertid ikke utført randomiserte dobbeltblinde placebokontrollerte studier som undersøker disse behandlingene.
En retrospektiv studie viste ikke at plasmaferese endret sjansen for full restitusjon og tiden det tok å løse ataksi og oftalmoplegi; videre påvirket intervallet fra oppstart til oppstart av plasmaferesebehandling ikke tid til bedring eller alvorlighetsgraden av symptomene ved oppstart. En kasusrapport indikerer imidlertid at plasmaferese er indisert når dyp ataksi, motorisk og respiratorisk svekkelse er tilstede.21
Pasienter bør overvåkes nøye for risiko for å utvikle alvorlige systemiske komplikasjoner som øvre respirasjonssvikt. Studier viser ingen signifikant forbedring i utvinningstiden MED IV IgG eller plasmaferesebehandling ved MFS, så overvåking kan være en utøvers beste alternativ.
mens sjeldne, tilstanden trenger ikke gå udiagnostisert. Ved å gjenkjenne de viktigste kliniske funksjonene, kan utøvere avsløre årsaken til pasientens symptomer og få tillit til full gjenoppretting. Dr. Wang og Cantrell er optikere ved Orlando VA Medical Center. Dr. Cali er en stab optometrist På Lee County VA Clinic. Forfatterne ønsker å takke Joseph Miller, Od, Paul Gruosso, OD, Og Vanessa Santos, OD, for hjelp med dette manuskriptet.
1. Collier J. Perifer nevritt: Morisa forelesninger. Edinburgh Med J. 1932: 39: 601-18.
2. Fisher M. en uvanlig variant av akutt idiopatisk polyneuritt(syndrom oftalmoplegi, ataksi og arefleksi). N Eng J Med. 1956:255:57-65.
3. Lo YL, et al. Klinisk og immunologisk spektrum Av Miller Fisher syndrom. Muskel Nerve. 2007:36(5):615-27.
4. Mori M, Kuwabara S, Fukutake T, et al. Kliniske egenskaper Og prognose Av Miller Fisher Syndrom. Nevrologi. 2001:56(8): 1105-6.
5. Mori M, Kuwabara S, Fukutake T, et al. Plasmapharesis Og Miller Fisher syndrom: Analyse av 50 påfølgende tilfeller. J Neurol Neurosurg Psych. 2002:72:680.
6. Yuan CL, Wang YJ, Tsai CP. Miller Fisher syndrom: en sykehusbasert retrospektiv studie. Euro J Neurol. 2000:44(2):79-85.
7. Cheng BC, Chang WN, Chang CS et al. Guillain-Barré syndrom i sør-Taiwan: Kliniske egenskaper, prognostiske faktorer og terapeutiske resultater. Euro J Neurol. 2003:10 (6):655-62.
8. Berlit P, Rakicky J. Miller Fisher syndrom. Gjennomgang av litteratur. J klinisk nevro-oftalmologi. 1992:12:57-63.
9. Liu RK, Tang LM, Cheng SY, et al. Guillain-Barré syndrom I Taiwan: en klinisk studie av 167 pasienter. J Neurol Neurosurg Psych. 1997:63:494-500.
10. Tatsomoto M, Odaka M, Hirata K, Yuki N. Isolert abducens parese som en regional variant Av Guillain-Barré Syndrom. J Neurol Sci. 2006:243:35-8.
11. Weiss JA, Hvit JC. Korrelasjon av 1a afferent ledning med Ataksi Av Fisher syndrom. Muskel Nerve. 1986:9:327-32.
12. Das P, Biswash S, et al. Miller Fisher variant av guillain-barré syndrom: en saksrapport og klinisk gjennomgang. Bangabandhu Sheikh Mujib Medisinsk Univer J. 2012: 5 (1): 69-71
13. Kornberg AJ, Pestronk A, Blume GM, et al. Selektiv farging av cerebellar molekylær lag av serum IgG Av Miller Fisher og relaterte syndromer. Nevrologi. 1996:47:1317-20.
14. Inoue N, Koh C, Iwahashi T. Påvisning av serum anticerebellar antistoffer hos pasienter Med Miller Fisher Syndrom. Euro J Neurol. 1999:42:230-4.
15. Barontini F, Di Lollo S, Maurri S, Lambruschini P. Lokalisering av den patologiske prosessen I Miller Fisher Syndrom. Italia J Neurol Sci. 1992:13:221-5.
16. Koga M, Yuki N, Takahashi M, et al. Nær tilknytning av iga-anti-gangliosidantistoffer med antecedent Campylobacter jejuni-infeksjon i guillain-Barré og Fishers syndromer. J Neuroimmunol. 2003:141:112-7.
17. Guiloff RJ. Perifer nervedannelse I Miller Fisher syndrom. J Neurol Nevrokirurg Psychiat. 1977:40:801-7.
18. Chikakiya H, Kunishige M, Yoshino H, et al. Forsinket motorisk og sensorisk nevropati hos en pasient med hjernestammen encefalitt. J Neurol Sci. 2005:234:105-8.
19. Arakata Y, Yoshimuro M, Kobayashi S, et al. Bruk av intravenøs immunoglobulin I Miller Fisher syndrom. Hjernen Utvikler J. 1993:15:231-3.
20. Matsumoto H, Kobayashi O, Tamura K, et al. Miller Fisher syndrom med forbigående koma: sammenligning med bickerstaffs hjernestamme encefalitt. Hjernen Utvikler J. 2002: 24: 98-101.
21. Yeh JH, Chen WH, Chen JR, Et al. Miller Fisher syndrom med sentral involvering: vellykket behandling med plasmaferese. Therap Aferese Dialyse J. 1999: 3: 69-71.
22. Papanikolaou T, Kath G, Boothman B, et al. Saksrapport: akutt bilateral oftalmoparese med pupilær arefleksisk mydriasis i Miller-Fisher syndrom behandlet med intravenøst immunglobulin. J Oftalmol. 2010; Artikkel-ID 291840.
23. Sandler RD, Hoggard N, Hadjivassiliou M. Miller-Fisher syndrom: er ataksi sentral eller perifer? Cerebellum Ataksier. 2015:2:3.
24. Ejma M, Waliszewska-Prosół M, Hofman A, Et al. Progressiv Subakutt Miller-fisher syndrom vellykket behandlet med plasmaferese. Polsk J Neurol Neurosurg. 2015;49(2):137-8.
25. San-Juan AV, Mart5ez-Herrera JF, Moreno Garcauka J, Et al. Miller Fisher syndrom: 10 års erfaring i et tredje nivå senter. Euro Neurol. 2009; 62: 149-54
26. Snyder LA, Rismondo V, Miller NR. Fisher-varianten Av Guillain-Barré syndrom (Fisher syndrom). J Neuroophthalmol. 2009 Desember; 29 (4): 312-24.
27. M, M, M, M, m, et al. Bickerstaff hjernestamme encefalitt og fisher syndrom danner et kontinuerlig spektrum: klinisk analyse av 581 tilfeller. J Neurol. 2008;255:674-82.
28. Yuki N. Akutt parese av ekstraokulære muskler assosiert Med IgG anti-GQ1b antistoff. Ann Neurol 1996; 39: 668-72.