Lavspenningsglaukom: En Oksymoron i Oftalmologi
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (Vis forfattertilknytning)
Foreslått sitat for denne artikkelen: Costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. Lavspenningsglaukom: En Oksymoron I Oftalmologi. Forrige Kronisk Dis 2019;16: 180534. DOI:http://dx.doi.org/10.5888/pcd16.180534external ikon.
begrepet glaukom refererer til en gruppe okulære tilstander preget av progressiv optisk nerveskade og tap av synsfelt (1). Glaucomatøs optisk nevropati skyldes det progressive tapet av retinale ganglionceller; forhøyet intraokulært trykk (IOP) er en viktig risikofaktor. IOP kan virke direkte, mekanisk eller indirekte, ved å påvirke blodtilførselen (2). Faktorer som påvirker utviklingen av glaucomatøs optisk nevropati inkluderer eldre alder, avansert sykdomsstadium, høyere IOP og skiveblødninger (3). Hos pasienter med primær åpenvinklet glaukom (POAG) er den økte motstanden mot vandig utstrømning gjennom trabekulært meshwork den viktigste skyldige for forhøyet IOP. Til tross for tilstrekkelig kontroll av IOP kan imidlertid glaucomatøs optisk nevropati ofte fortsette å utvikle seg. Dermed er faktorer som ikke er relatert TIL IOP anerkjent, med det viktigste å være en reduksjon i blodtilførselen til optisk nerve (4).
Andre faktorer som ikke er relatert til IOP inkluderer glutamattoksisitet, oksidativt stress, autoimmunitet og vaskulær dysregulering (3). LAVSPENT drderamus (LTG) er definert som en form for drderamus som tett etterligner POAG, men IOP-nivåene er innenfor det normale området og den sannsynlige patogenesen er vaskulær.de kontroversielle spørsmålene er 1) ER LTG en sykdom på SPEKTERET AV POAG (på venstre side av fordelingen AV IOP, på laveste nivå)?, 2) er optisk skiveutseende sekundært til optisk nervehypoperfusjon på grunn av vaskulære sykdommer?, eller 3) SKAL LTG inkluderes i et spekter av medfødte og oppkjøpte optiske nevropatier som kan simulere glaucomatøs optisk nevropati?
Top
Er Lavspenningsglaukom En Sykdom på Spekteret Av Primær Åpenvinklet Glaukom?
Da Albrecht von Graefe i 1857 beskrev en form for glaukom som manifesterte skade på optisk nervehodet og en åpen fremre kammervinkel, med IOP innenfor referanseområdet, ble digital palpasjonstonometri ansett som gullstandarden. Hvis han hadde brukt en avtrykkstonometer til å måle iop, ville den store mangelen på tonometri ha vært at den fordrev så mye væske ved kontakt med øyet at de målte avlesningene ville være svært variable og unøyaktige. Omvendt, hvis han hadde brukt innrykkstonometri, ville det ikke ha vurdert feilklassifisering som følge av tilstedeværelsen av en tynn sentral hornhinne (1). MANGE DIAGNOSER av LTG var for øyne med tynne hornhinner og var basert på falske lave verdier for IOP, et funn som tviler på DIAGNOSEN LTG (5). Videre må fravær av forhøyet IOP påvises ved målinger utført mer enn en gang eller på dagtid, siden IOP viser daglige og nattlige svingninger hos friske personer, og enda mer hos pasienter MED POAG eller LTG (6). For variasjoner i IOP kan det skilles mellom 3 POPULASJONER AV LTG-pasienter: pasienter uten iop-fluktuasjoner, pasienter med diurnal iop-akrofase (toppen eller toppen av en syklus) og pasienter med nattlig IOP-akrofase (7). Pasienter i de 2 siste kategoriene bør betraktes som sanne POAG-pasienter i stedet FOR LTG-pasienter, hvor glaucomatøs optisk nevropati oppstår til tross for normal IOP. Det er sannsynlig at pasienter med døgnlig eller nattlig akrofase har blitt inkludert i studier basert på mekanisk teori; reduksjon av IOP kan bare forsinke progresjonen av synsfelttap hos disse pasientene (8). Data Fra Lavtrykksglaukom – Behandlingsstudien fremhevet IOPS rolle i LTG-patogenesen; progresjonen av synsfelttap ble redusert med 9,1% med timolol 0,5% og med 39,1% med brimonidin 0,2% etter 2 års behandling (8). I denne studien ble imidlertid iop-verdier registrert utelukkende på dagtid. Således er det ukjent om pasienter med verre synsfelt hadde iop nattlig akrofase. Andre studier på asymmetrisk LTG rapporterte at øyet med høyere iop viser større glaucomatøs skade enn øyet med lavere iop, som opprettholder IOPS rolle i patogenesen (9). Likevel, i alle disse kliniske studiene ble iop målt bare i kontortiden; dermed ble oppførselen til nattlig iop ikke registrert. En nylig studie hvor nychthemeral iop-kurver ble evaluert med en telemetrisk sensor viste en nattlig akrofase med IOP-pigger hos PASIENTER MED LTG, selv om disse toppene var på signifikant lavere nivåer enn toppene funnet hos pasienter med POAG (7). Denne studien rapporterte at IOP toppet om natten hos 40% til 80% av pasientene med normalspenningsglaukom, og mønsteret hos disse pasientene var lik mønsteret hos pasienter med POAG. I 24-timers kurver hadde pasienter MED LTG og POAG mer uttalt mønstre av IOP om kvelden og natten enn om morgenen, med flere topper og større iop-svingning om natten enn om kvelden (7). Andre faktorer kan bekrefte hypotesen om et primært iop-relatert mekanisk stress i LTG, for eksempel tilstedeværelsen av endringer i de vandige humorutstrømningsbanene som ligner DE som forekommer I POAG (10).
hos pasienter HVOR LTG kan betraktes som en sykdom på SPEKTERET AV POAG, må diagnostiske og terapeutiske strategier som ligner på pasienter med hyperbarisk glaukom, implementeres ved hjelp av en øyelege (Figur).
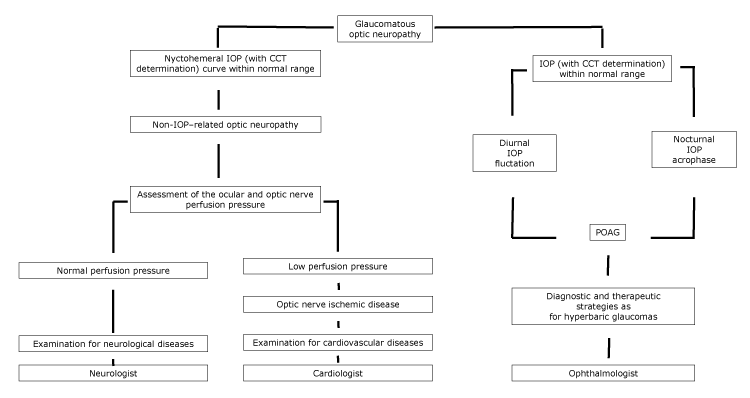
Figur.
Foreslått flytskjema av optisk nevropati, med spesialist henvisning, i henhold til nychthemeral iop egenskaper. Forkortelser: CCT, sentral hornhinnetykkelse; iop, intraokulært trykk; POAG, primær åpenvinklet glaukom.
Topp
Er Optisk Skiveutseende Sekundært Til Optisk Nervehypoperfusjon På Grunn av Vaskulære Sykdommer?
hos pasienter med LTG og normale nychthemeral iop-kurver kan ikke mekaniske faktorer være ansvarlige for optisk nevropati; trykkuavhengige faktorer kan være involvert, med vaskulære endringer som potensielt er de viktigste (5). En glaucomatøs-lignende optisk nevropati kan observeres hos pasienter med tidligere kardiovaskulær hendelse eller med kronisk aterosklerose eller obstruktiv arteriell sykdom (11). Redusert blodstrømningshastighet i retrobulbar arterier og i cerebral sirkulasjon, lavt diastolisk blodtrykk og mindre sentral retinal kardiameter er også observert hos PASIENTER med LTG (5). Hos disse pasientene skyldes patogenesen av sykdom et svekket okulært perfusjonstrykk, hovedsakelig knyttet til primær vaskulær dysregulering eller til en generalisert dysfunksjon av det endoteliale eller autonome nervesystemet (5,11). Det er imidlertid uklart om disse faktorene var årsaken eller resultatet av optisk nevropati. FRA et klinisk synspunkt VISER LTG en høyere forekomst av skiveblødninger og er hyppigere forbundet med vaskulære sykdommer som migrene, obstruktiv søvnapne eller Raynauds syndrom enn MED IOP (5). Til slutt viser omtrent halvparten AV LTG-pasienter med pre-perimetrisk sykdom skadeprogresjon til tross for normale IOP-verdier (12). Alle disse funnene tyder på den viktige rollen som vaskulær dysregulering.
hos pasienter med hjerte-og karsykdommer kan kopping av optiske plater ha en tendens til ikke å utvikle seg dersom den underliggende årsaken til optisk nevropati er kontrollert. LTG-pasienter kan dessuten vise sirkumpapillær atrofi samt hjernebarkale mikroinfarkt, som er tegn på iskemi (5). Hos pasienter hvor vaskulære sykdommer induserer en optisk nervehypoperfusjon, må en komplett diagnostisk undersøkelse for kardiovaskulære sykdommer utføres ved hjelp av en kardiolog(Figur).
Top
SKAL LTG Inkluderes i Et Spekter Av Medfødte Og Ervervede Optiske Nevropatier som Kan Simulere En Glaucomatøs Optisk Nevropati?
når de hyppigste årsakene til kopping av optiske plater er utelukket, bør muligheten for nevrodegenerativ optisk nevropati vurderes. Disse tilfellene er de mest frustrerende, fordi optisk diskskade utvikler seg selv etter at IOP er senket. Mange medfødte og ervervede optiske nevropatier er inkludert i denne gruppen av tilfeller, og differensiering mellom glaucomatous og nonglaucomatous cupping kan være utfordrende selv for erfarne observatører (13). Blant de medfødte former for optisk diskkopping, megalopapilla, autosomal dominant optisk atrofi og leber arvelig optisk nevropati kan produsere en optisk diskutgravning som simulerer glaucomatøs optisk nevropati.
de oppkjøpte nevropatiene kan være sekundære til inflammatoriske, komprimerende, giftige og traumatiske årsaker. Optisk neuritt kan gi en økning av kopp-til-disk-forholdet som, selv om det er ensidig, kan forveksles med glaucomatøs optisk nevropati. Kompresjonslesjoner, inkludert meningeom, hypofyse-adenom, kraniofaryngiom og intern carotisar-aneurisme, kan føre til asymmetrisk optikeropphopning og feilaktig tilskrives LTG. Metanol og etambutol forgiftning kan produsere en bilateral optisk plate cupping lik glaucomatous optisk nevropati, sekundært til aksonal tap. Når en asymmetrisk forstørret kopp observeres, er det derfor nødvendig med ytterligere neuro-oftalmologisk undersøkelse (13).Til Slutt, blant forhold som fører til optisk diskkopping, har aldring en hovedrolle. Harju et al fant at graden av optisk diskkopping økte hos friske eldre studiedeltakere på grunn av fysiologisk fibertap. Deres studiepopulasjon var hensiktsmessig og representerte et sett med sunne øyne uten drderamus; i løpet av 11 års oppfølging utviklet ingen studiedeltakere visuelle feltendringer, og ingen signifikant økning i IOP ble registrert (14). I sistnevnte tilfelle må en komplett diagnostisk undersøkelse for nevrologiske sykdommer utføres ved hjelp av en nevrolog (Figur).Forbedringer i diagnostiske teknikker gjør det enklere enn før å klassifisere optisk diskkopping; en beskrivelse av optiske skiveegenskaper kombinert med avbildning av netthinnenervefiberlaget og optisk disktopografi tillater differensiering mellom glaucomatøs og nonglaukomatøs optisk diskkopping. Videre bidrar en nøye analyse av pasientens historie, sammen med morfologisk og funksjonell vurdering av optisk nerve, til å identifisere lidelser.BEGREPET LTG kan være en selvmotsigelse, et nostalgisk minne fra fortiden når en definert diagnose ikke var mulig. Å bruke begrepet er som å bruke ordet «feber» når det ikke er høy temperatur eller si festina lente («mer hast, mindre fart»). BEGREPET LTG kan være misvisende eller unøyaktig, fordi det refererer til et mekanisk problem med IOP, mens optisk diskkopping og synsfelttap i øyne med normalt intraokulært trykk skyldes andre faktorer. Derfor, i nærvær av optisk diskkopping med normal IOP, bør oftalmologer undersøke andre troverdige årsaker til optisk nerveskade i tillegg til intraokulært trykk.
Top
Bekreftelser
denne studien mottok ikke noe spesifikt tilskudd fra noen finansieringsbyrå i offentlig, kommersiell eller ideell sektor.
Topp
Forfatter Informasjon
Tilsvarende Forfatter: Luca Agnifili, MD, PhD, Oftalmologi Klinikk, Via dei Vestini, 66100, Chieti (CH), Italia. Telefon: +39-0871-358489. Epost: [email protected].
Forfatter Tilknytninger: 1 institutt For Medisin Og Helsefag, Universitetet I Molise, Campobasso, Italia. 2 Institutt For Medisin Og Aldring Vitenskap, Oftalmologi Klinikk, Universitet G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14-21. CrossRefexternal icon PubMedexternal icon
- De Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; Lavt trykk Glaukom Behandling Studiegruppe. Risikofaktorer for synsfeltprogresjon i lavtrykksglaukom behandlingsstudie. Er J Oftalmol 2012; 154 (4): 702-11. Cartwright Mj, Anderson DR. Korrelasjon av asymmetrisk skade med asymmetrisk intraokulært trykk i normalspenningsglaukom (lavspenningsglaukom). Arch Oftalmol 1988; 106 (7): 898-900. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top