低張力緑内障:眼科におけるオキシモロン
Ciro Costagliola,MD1;Luca Agnifiili,MD,Phd2;Leonardo Mastropasqua,MD2;Alfonso di Costanzo,MD1(view author affiliations)
この記事の引用を提案しました:Costagliola C,Agnifi L,Mastropasqua L,di Costanzo A.眼科… 2019年(平成16年)10月18日-5月34日に放送された。 DOI:http://dx.doi.org/10.5888/pcd16.180534externalアイコン。緑内障という用語は、進行性の視神経損傷および視野の喪失を特徴とする眼の状態の群を指す(1)。
緑内障という用語は、進行性の視神経損傷および視野の喪失を特徴とする眼の状態の群を指す(1)。 緑内障性視神経障害は、網膜神経節細胞の進行性の喪失によるものであり、眼内圧の上昇(IOP)が主要な危険因子の一つである。 IOPは、直接的に、機械的効果によって、または間接的に、血液供給に影響を及ぼすことによって作用することができる(2)。 緑内障性視神経障害の進行に影響を与える要因には、高齢、進行した病期、より高いIOP、および椎間板出血が含まれる(3)。 原発性開放隅角緑内障(POAG)の患者では、小柱メッシュワークを通る水性流出に対する耐性の増加が、IOPの上昇の主な原因である。 しかし,iopの適切な制御にもかかわらず,緑内障性視神経障害は頻繁に進行し続ける可能性がある。 したがって、IOPに関連しない要因が認識され、最も重要なのは視神経への血液供給の減少である(4)。IOPに関連しない他の要因には、グルタミン酸毒性、酸化ストレス、自己免疫、および血管調節不全(3)が含まれる。
IOPに関連しない他の要因には、グルタミン酸毒性、酸化ストレス、自己免疫、および血管調節不全がある。 低張力緑内障(LTG)は、POAGを密接に模倣する緑内障の一形態として定義されるが、IOPレベルは正常範囲内であり、そして考えられる病因は血管である。論争の的になっている質問は1)LTGはPOAGのスペクトル(IOPの分布の左側、最低レベル)の病気ですか?、2)視神経乳頭の外観は、血管疾患による視神経低灌流に二次的であるか?、または3)LTGは、緑内障性視神経障害をシミュレートすることができ、先天性および後天性視神経障害のスペクトルに含まれるべきですか?
トップ
低緊張緑内障は原発性開放隅角緑内障のスペクトル上の疾患ですか?
1857年にAlbrecht von Graefeが視神経頭部および開いた前房角に損傷を示す緑内障の形態を記述したとき、IOPは基準範囲内にあり、デジタル触診眼圧測定は金本 彼がIOPを測定するために印象眼圧計を使用していた場合、眼圧計の主な欠点は、測定された測定値が非常に可変で不正確であることを目に接触すると、それが非常に多くの流体を変位させたことであったであろう。 彼は圧痕眼圧測定を使用していた場合、逆に、それは薄い中央角膜(の存在に起因する誤分類を考慮していないだろう1)。 LTGの多くの診断は、薄い角膜を有する眼に対するものであり、IOPの偽の低い値に基づいていた、LTGの診断にいくつかの疑問を投げかける所見(5)。 さらに、iopは健常者では日中および夜間の変動を示し、POAGまたはLTG患者ではさらに多くの変動を示すため、iopの上昇の欠如は、複数回または昼間に行われた測定で発見されなければならない(6)。 IOPの変動については、LTG患者の3つの集団を区別することができる:IOP変動のない患者、日周IOPアクロファーズ(サイクルの頂上またはピーク)を有する患者、およ 最後の2つのカテゴリーの患者は、正常なIOPにもかかわらず緑内障性視神経障害が起こるLTG患者ではなく、真のPOAG患者とみなされるべきである。 日中または夜間の好中球を有する患者は、機械的理論に基づく研究に登録されている可能性が高い; IOPの減少は、これらの患者においてのみ視野喪失の進行を遅くする可能性がある(8)。 低圧緑内障治療研究からのデータは、LTG病因におけるIOPの役割を強調し、視野損失の進行は、治療の9.1%チモロール0.5%と39.1%ブリモニジン0.2%で2年後に減少した(8)。 しかし,本研究では,IOP値は昼間のみ記録した。 したがって、より悪い視野を有する患者がiop夜間アクロファーズを有していたかどうかは不明である。 非対称LTGに関する他の研究では、iopが高い眼は、iopが低い眼よりも緑内障性の損傷が大きく、病因におけるiopの役割を維持することが報告されています(9)。 しかし、これらのすべての臨床試験では、IOPは営業時間中にのみ測定されたため、夜間IOPの行動は記録されなかった。 これらのスパイクはPOAG患者の間で見つかったスパイクよりも有意に低いレベルであったが、nychthemeral IOP曲線は、テレメトリックセンサーで評価された最近の研究は、LTG患者のIOPスパイクと夜行性のアクロフェーズを示した(7)。 この研究では、正常緊張緑内障患者の40%から80%で夜間にIOPがピークに達し、これらの患者のパターンはPOAG患者のパターンと同様であったことが報告された。 24時間曲線では、LTGとPOAGの患者は、夕方よりも夜と夜にIOPのより顕著なパターンを持っていた、より多くのピークと夕方よりも夜の間に大きなIOP変動(7)。 他の要因は、POAGで起こるものと同様の房水流出経路の変化の存在のような、LTGにおける一次IOP関連の機械的ストレスの仮説を裏付けることができる(1 0)。
LTGがPOAGのスペクトル上の疾患と考えることができる患者では、眼科医の助けを借りて、高圧緑内障患者と同様の診断および治療戦略を実施しなけ
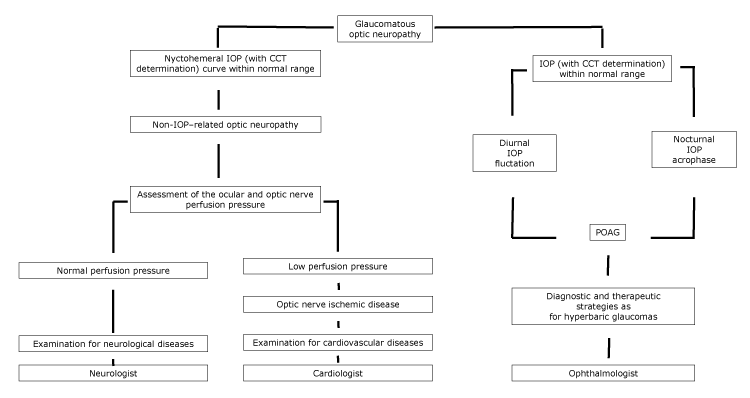
図。
視神経障害のフローチャートを提案しました,専門家の紹介と,nychthemeral IOP特性に応じて. 略語:CCT、中心角膜厚;IOP、眼圧;POAG、原発性開放隅角緑内障。
トップ
視神経乳頭の外観は、血管疾患による視神経低灌流に続発していますか?
LTGおよび正常なnychthemeral IOP曲線を有する患者では、機械的要因は視神経障害の原因となることはできず、圧力に依存しない要因が関与しており、血管変化が潜在的に最も重要である可能性がある(5)。 緑内障様視神経障害は、心血管イベントの病歴または慢性アテローム性動脈硬化症または閉塞性動脈疾患を有する患者において観察され得る(11)。 Ltg患者では、球後動脈および脳循環における血流速度の低下、拡張期血圧の低下、および網膜中心血管直径の低下も観察されている(5)。 これらの患者では、疾患の病因は、主に一次血管調節不全または内皮または自律神経系の一般化された機能不全に関連する眼灌流圧の障害に起因する(5,11)。 しかし,これらの要因が視神経障害の原因であったのか,それとも結果であったのかは不明である。 臨床的観点から、LTGは椎間板出血の発生率が高く、iopよりも片頭痛、閉塞性睡眠時無呼吸症候群、またはレイノー症候群などの血管疾患とより頻繁に関連しています(5)。 最後に、perimetric前疾患を有するLTG患者の約半分は、正常なIOP値にもかかわらず、損傷の進行を示している(12)。 これらの所見はすべて血管調節不全の重要な役割を示唆している。
心血管疾患の患者では、視神経障害の根本的な原因が制御されている場合、視神経乳頭カッピングが進行しない傾向がある可能性があります。 さらに、LTG患者は、毛細血管萎縮および虚血の徴候である大脳皮質微小梗塞を示す可能性がある(5)。 血管疾患が視神経低灌流を誘発する患者では、心臓病専門医の助けを借りて、心血管疾患の完全な診断検査を実施しなければならない(図)。LTGは、緑内障性視神経障害をシミュレートすることができる先天性および後天性視神経障害のスペクトルに含めるべきですか?
Top
LTGは、緑内障性視神経障害をシミュレートすることができる先天性および後天性視神経障害のスペクトルに含める必要がありますか?
視神経乳頭カッピングのより頻繁な原因が除外されている場合は、神経変性性視神経障害の可能性を考慮する必要があります。 これらの症例は,iopが低下した後でも視神経乳頭損傷が進行するため,最もイライラする。 多くの先天性および後天性視神経障害は、ケースのこのグループに含まれており、緑内障とnonglaucomatousカッピングの分化は、経験豊富なオブザーバー(ためにも挑戦するこ 視神経乳頭カッピングの先天性形態の中で、megalopapilla、常染色体優性視神経萎縮、およびLeber遺伝性視神経障害は、緑内障性視神経障害を模擬した視神経乳頭掘削を生後天性神経障害は、炎症性、圧迫性、毒性、および外傷性の原因に続発している可能性がある。
視神経炎は、一方的ではあるが、緑内障性視神経障害と混同される可能性のあるカップ対ディスク比の増加を生じる可能性がある。 髄膜腫,下垂体腺腫,頭蓋咽頭腫,および内頚動脈動脈りゅうを含む圧縮病変は,非対称視神経乳頭カッピングを引き起こし,LTGに誤って起因する可能性がある。 メタノールおよびエタンブトール中毒は、緑内障性視神経障害に類似した両側視神経乳頭カッピングを生成し、軸索損失に続発する可能性がある。 したがって、非対称の拡大カップが観察される場合、さらなる神経眼科的調査が必要である(13)。
最後に、視神経乳頭カッピングにつながる条件の中で、老化が主な役割を持っています。 Harjuらは、生理的繊維損失のために、健康な高齢の研究参加者では視神経乳頭カッピングの程度が増加することを見出した。 彼らの研究集団は適切であり、緑内障のない健康な目のセットを表していた;フォローアップの11年間を通じて、研究参加者は視野の変化を開発せず、IOPの有意な上昇は記録されなかった(14)。 この後者の場合、神経科医の助けを借りて、神経疾患の完全な診断検査を実施しなければならない(図)。
診断技術の改善は、それが簡単に視神経乳頭カッピングを分類するために以前よりも作ります;網膜神経線維層と視神経乳頭地形のイメージングと組 さらに、視神経の形態学的および機能的評価とともに、患者の病歴を慎重に分析することは、障害を特定するのに役立つ。LTGという用語は、定義された診断が不可能であった過去の懐かしい記憶である矛盾である可能性があります。
LTGという用語は、定義された診断が この用語を使用することは、高温がないときやfestina lente(”より急いで、より少ない速度”)と言っているときに”発熱”という言葉を使用するようなものです。 LTGという用語は、IOPの機械的問題を指すため、誤解を招くか不正確である可能性がありますが、正常な眼圧を有する眼の視神経乳頭カッピングおよび視野損失は他の要因によって引き起こされる。 したがって、正常なIOPと視神経乳頭カッピングの存在下で、眼科医は眼圧以外の視神経損傷の他のもっともらしい原因を調査する必要があります。
トップ
謝辞
この研究は、公共、商業、または非営利セクターの資金調達機関から特定の助成金を受けていませんでした。
トップ
著者情報
対応する著者:Luca Agnifiili、MD、PhD、眼科クリニック、via dei Vestini、66100、Chieti(CH)、イタリア。 電話:+39-0871-358489. 電子メール:[email protected].
著者の所属:1モリーゼ大学、カンポバッソ、イタリアの医学と健康科学の部門。 2大学眼科クリニック医学-老化科学部 d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14–21 CrossRefexternal icon PubMedexternal icon
- De Moraes CG,Liebmann JM,Greenfield DS,Gardiner SK,Ritch R,Krupin T;低圧緑内障治療研究グループ。 低圧緑内障治療研究における視野進行の危険因子。 Am J Ophthalm2012;154(4):702-11. Crossrefexternal icon PubMedexternal icon
- Cartwright MJ,Anderson dr.正常緊張緑内障(低緊張緑内障)における非対称眼圧と非対称損傷の相関。 Arch Ophthalmol1988;106(7):898-900。 CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top