guarda gli Ultimi articoli
Abstract
Fondo: polmonare l’endometriosi è una delle relativamente rare forme di extragenital endometriosi e, in conformità alle proprie clinico-patologica sintomi è considerato nei termini di “toraciche endometriosi, sindrome di”, vale a dire quando il funzionamento endometrio è trovato nella pleura, membrana, viae respiratoriae o parenchima polmonare stesso.
Obiettivi: sono stati osservati 42 casi di questa malattia. L’età dei pazienti variava da 16 a 61 anni, quindi la media era di 40,5 ± 0,4 anni.
Risultati: Nella maggior parte dei casi l’endometriosi ha interessato il diaframma ed è stata accompagnata da un pneumotorace con il corrispondente complesso di sintomi, mentre i focolai polmonari si sono verificati più rari, essendo asintomatici o fingendo qualche patologia chirurgica e di altro tipo. L’intervento chirurgico e lo studio istologico sono stati cruciali per verificare la diagnosi. I recettori del progesterone e degli estrogeni e la produzione di Ki-67 sono stati rilevati immuno-istochimicamente nel tessuto endometrioide dei focolai polmonari.
Conclusione: L’uso dei metodi istologici e immuno-istochimici completi è stato richiesto per rendere più affidabile la diagnosi finale dell’endometriosi polmonare. Ha un grande significato pratico essendo uno dei più importanti pre-requisiti per la prescrizione di un trattamento adeguato.
parole Chiave
toracica endometriosi, sindrome di, extragenital endometriosi, polmonare endometriosi, membrana di lesione, pneumotorace, istologiche verifica della diagnosi
Introduzione
l’Endometriosi è una crescita di tessuto simile all’endometrio al di fuori della cavità uterina, che è accompagnata da una reazione infiammatoria cronica, che porta nella maggior parte dei casi allo sviluppo di una sindrome di dolore e/o infertilità. Attualmente, è una delle più comuni malattie ginecologiche. Questa patologia si verifica nel 2-10% delle donne in età riproduttiva e quasi nel 50% delle donne con infertilità .
Una delle forme relativamente rare dell’endometriosi è caratterizzata dallo sviluppo del tessuto endometriale al di fuori del sistema riproduttivo. I fuochi extragenitali possono esistere indipendentemente sia come formazioni separate che come componenti delle lesioni concomitanti . I casi dell’endometriosi extragenitale fanno il 6-8% del numero totale dell’endometriosi osservata. Tra gli organi estranei al sistema riproduttivo, ci sono l’intestino, il tratto urinario e i polmoni che sono più frequentemente colpiti .
Hart fu il primo a diagnosticare l’endometriosi polmonare (PE) postumo nel 1912. Osservò in una donna, di 72 anni, numerosi nodi subpleurici che variavano dalle dimensioni di un pisello a quelle di una noce. L’esame istologico ha mostrato adenomiosi di origine uterina; un tumore nell’utero del paziente è stato rimosso 22 anni prima .
Nell’ultimo decennio il numero di pubblicazioni sull’endometriosi è notevolmente aumentato. Il concetto di “sindrome da endometriosi toracica” (TES) è stato sviluppato e utilizzato nei casi in cui l’endometrio funzionante si trova nella pleura, nel diaframma, nelle vie respiratorie o nel parenchima polmonare stesso .
Channabasavaiah e Joseph hanno presentato i risultati di un’analisi di 110 casi clinici di endometriosi intratoracica istologicamente verificata pubblicati tra il 2001 e il 2007. Legras et al. hanno studiato retrospettivamente 229 casi di pneumotorace nelle donne descritte nella letteratura specialistica scritta in inglese dal 2000 al 2011 e affermano che la TES viene diagnosticata in 54 casi (24 per cento).
La questione di come un endometrio funzionante entra nel petto rimane ancora aperta . Sampson è stato il primo a suggerire che l’endometrio viene trasferito dalla cavità uterina a quella addominale attraverso le tube di Falloppio attraverso la cosiddetta “mestruazione retrograda”, cioè lo scarico di una certa quantità di sangue nella cavità pelvica durante le mestruazioni. Questo tipo di reflusso si verifica in un gran numero di donne sane . Sampson ha anche ipotizzato un’esistenza dell’endometriosi metastatica, o embolica, che consente di speculare sulle vie ematogene della propagazione dell’endometriosi. Hobbs e Bortnick hanno confermato questa ipotesi introducendo sperimentalmente la sospensione dell’endometrio nelle vene dell’orecchio dei conigli, che ha portato allo sviluppo dell’EP nel 79% dei casi.
La TES si manifesta più spesso nel pneumotorace ricorrente, nell’emottisi, nella tosse o nel dolore toracico e più raramente nell’emotorace associato al ciclo mestruale . Il PE è una delle forme più rare del TES. Le manifestazioni cliniche più importanti del primo sono tosse, emottisi e una sensazione di pesantezza al petto (un sintomo di “pelliccia pesante”) che si verificano durante le mestruazioni, ma non necessariamente in ogni ciclo mestruale.
Secondo la letteratura, il pneumotorace associato al TES si trova in circa il 10-24% delle donne con pneumotorace spontaneo .
L’esame del torace a raggi X (principalmente HRCT) rivela quattro varianti della patologia: opacità lineari o reticolari, piccoli noduli, spazi aerei cistici, setti alveolari ispessiti. Questi risultati radiologici, in particolare quelli combinati con un’emottisi e dolore toracico sono spesso considerati come un’evidenza di una natura tubercolare o neoplastica della lesione polmonare.
Una lesione del diaframma viene solitamente rilevata per caso durante un intervento chirurgico a causa di pneumotorace. Prima dell’intervento questa patologia viene rilevata molto raramente a causa di una limitata estensione delle lesioni e della bassa risoluzione dei metodi radiologici.
Quasi senza eccezioni, la malattia colpisce un centro tendinoso della cupola del diaframma destro e può apparire in due tipi. Il primo assume la forma di impianti endometriosi blu o viola sotto la pleura parietale fino a 5 mm di dimensione. I secondi sono difetti rotondi o a fessura nel diaframma.
La mancanza di sintomi specifici, di marcatori di laboratorio e di schemi radiologici caratteristici rende difficile la diagnosi preoperatoria di PE. Spesso è finalmente diagnosticato solo dopo una conferma dai metodi istologici, tra loro l’immuno-istochimica, compreso espressione di recettori di progesterone e dell’estrogeno .
Pertanto, l’intervento chirurgico è spesso necessario a scopo diagnostico e terapeutico. Sebbene l’operazione verifichi di norma la diagnosi e rimuova eventuali lesioni endometriali eterotopiche, questo tipo di trattamento rimane incompleto senza una terapia ormonale soppressiva. Mira a un blocco dell’ovulazione, a una soppressione della secrezione di estrogeni e alla soppressione della crescita epiteliale nel fuoco endometriale .
Un numero relativamente piccolo di casi di TES descritti nella letteratura specialistica mondiale e la mancanza del suo quadro clinico patognomonico ci hanno spinto a riassumere la nostra esperienza nella diagnostica e nel trattamento di questa malattia.
Metodi
Abbiamo analizzato 42 casi di TES osservati nei nostri ospedali nel periodo dal 2004 al 2016. L’età dei pazienti variava da 16 a 61 anni, quindi la media era di 40,5±0,4 anni.
35 pazienti sono stati ospedalizzati a causa di uno pneumotorace spontaneo, 3 con masse tumorali arrotondate, 1 con una cisti e 3 con un’infiltrazione nel tessuto polmonare. Significativamente, in 41 pazienti il processo patologico è stato localizzato nel polmone destro.
Risultati
Le principali lamentele di tutti i pazienti ospedalizzati sono elencate nella Tabella 1.
Tabella 1. Complaints of patients with the thoracic endometriosis syndrome
|
Complaints |
Patients (n=42) |
|
|
abs. number |
per cent |
|
|
Chest pain |
85,7 |
|
|
Dyspnea |
73,8 |
|
|
Dry cough |
50,0 |
|
|
Infertility |
14,3 |
|
|
Emottisi |
9,5 |
|
Nella maggior parte dei casi, c’era un dolore al petto (85.7 per cento); l’emottisi è stato trovato meno spesso (9,5 per cento). La dispnea è stata osservata solo in 31 pazienti con pneumotorace; 6 donne hanno sofferto di infertilità. Nell’anamnesi, 5 pazienti avevano mioma uterino e c’era una cisti endometriale dell’ovaio in 2 pazienti.
HRCT del torace rilevato ombre arrotondate nei polmoni (3 casi), infiltrati con cavità a parete sottile (6 casi), cisti polmonare (1 caso), bolle di vario diametro (6 casi) e una massa nella regione paravertebrale considerata come un neurinoma (1 caso) (Figura 1). Allo stesso tempo non sono state rilevate variazioni nel tessuto polmonare in 26 casi su 42 (61,9% dei pazienti).
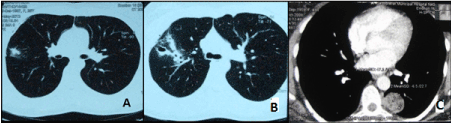
Figura. 1. Scansioni toraciche HRCT di pazienti con endometriosi polmonare A-infiltrazione del tessuto polmonare; B-piccole cavità; C-noduli periferici.
Sfortunatamente, un esame preoperatorio non ci consente di suggerire il TES in ogni caso, poiché l’espressione CA-125 non ne indica nemmeno la possibilità. Allo stesso tempo, un’analisi retrospettiva dei dati postoperatori ha suggerito che esisteva un prerequisito essenziale per questa diagnosi.
Le diagnosi pre-operative sono state le seguenti: pneumotorace spontaneo primario in 35 casi, tubercolosi polmonare infiltrativa in 3 casi, emosiderosi polmonare, neurinoma del mediastino, tumore polmonare e cisti polmonare – ciascuna in una.
L’intervento chirurgico è stato eseguito in 37 pazienti su 42. Di quelle donne 35 con pneumotorace, 30 (85.7 per cento) sono state operate. La resezione polmonare atipica è stata eseguita in 27 casi (90% dei pazienti), la pleurectomia costale in 28 casi (93,3%) e la resezione del centro del tendine del diaframma in 25 casi (83,3%).
Di 7 pazienti senza pneumotorace 6 sono stati sottoposti alla resezione polmonare atipica e 1 alla lobectomia.
In tutti i casi è stato eseguito un esame istologico del materiale chirurgico. Le sezioni di paraffina sono state colorate con ematossilina ed eosina, blu alciano e picrofuchsina di van Gieson. L’immuno-istochimica è stata eseguita utilizzando anticorpi contro i recettori del progesterone e degli estrogeni e anticorpi monoclonali del topo contro Ki-67 e bcl 2 (Dako, Danimarca).
Nel correlare i dati clinici e istologici, il TES è stato diagnosticato in tutti i casi e può essere suddiviso nelle seguenti categorie: perforazione della cupola destra del diaframma con impianti endometriali istologicamente identificati (6 pazienti); eterotopie endometriali intrapolmonari sotto forma di nodi, infiltrati e cisti( 11 pazienti); lesioni multifocali del polmone e del diaframma (1 paziente). Una perforazione della cupola destra del diaframma senza endometrio istologicamente identificato (“diaframma poroso”) è stata osservata in 24 casi.
La valutazione macroscopica dei polmoni rimossi ha rilevato cisti con materiale marrone scuro (6 casi). Le pareti delle cisti erano spesse, la loro superficie interna liscia (5 casi) o con escrescenze papillari (1 caso). 5 osservazioni rimanenti hanno rivelato piccoli focolai di emorragia nelle aree subpleuriche.
L’esame microscopico ha rilevato numerosi gruppi di ghiandole endometriali con uno stroma citogenico. La struttura di queste ghiandole corrispondeva a varie fasi del ciclo mestruale 9 (vale a dire. una fase di proliferazione o secrezione) presentata in quantità diverse. Il tipo endometriale di epitelio delle ghiandole era solitamente pseudostratificato, appiattito o colonnare; i nuclei cellulari erano situati ai diversi livelli; il citoplasma conteneva gocce segrete; qua e là sono stati notati alcuni segni di desquamazione dell’epitelio. Nella lumina alveolare e nell’interstizio polmonare sono stati spesso trovati depositi di emosiderina. Lo stroma ghiandolare era rappresentato da cellule allungate con nuclei a forma di fuso, in alcuni punti con caratteristiche di decidualizzazione (Figura 2). In 5 casi è stata osservata una trasformazione cistica delle ghiandole insieme a emorragie intorno a loro. Alcuni depositi di emosiderina e una trasformazione fibroblastica di uno stroma citogenico erano evidenti nella maggior parte dei casi.
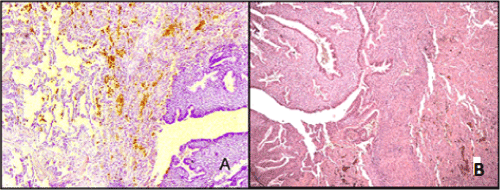
Figura. 2. Endometriosi polmonare. A-isole di proliferazione delle ghiandole endometriali. Nella lumina alveolare ci sono depositi di emosiderina. Ematossilina ed eosina colorazione( X 100); B – proliferante epitelio delle ghiandole con gocce segrete nel citoplasma. Stroma con caratteristiche di decidualizzazione. Colorazione di ematossilina ed eosina (X 160).
In tutti i casi è stato eseguito lo studio immuno-istochimico. Ha rivelato l’espressione dei recettori del progesterone e dell’estrogeno nell’epitelio della ghiandola e nelle cellule dello stroma citogenico (Figura 3 A, B), nonché l’espressione dell’oncoproteina bcl-2 nell’epitelio della ghiandola e l’attività proliferativa moderata (Ki-67) nello stroma citogenico (Figura 3 C).
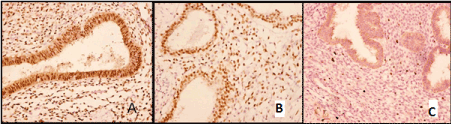
Figura. 3. Endometriosi polmonare: A-espressione ai recettori del progesterone nelle cellule epiteliali ghiandolari( X200); B – identico ai recettori degli estrogeni (X200); Espressione C – Ki-67 nello stroma citogenico (X100).
Di seguito sono riportati due esempi delle nostre osservazioni.
Esempio 1. Paziente F., 52 anni. La diagnosi clinica era un tumore del lobo inferiore del polmone destro. Sei anni prima, l’estirpazione dell’utero senza appendici è stata eseguita sul conto del mioma dell’utero con adenomiosi; il paziente soffriva di infertilità. 6 anni dopo l’intervento ci sono state lamentele su dolori periodici doloranti al petto, tosse ed emottisi. La radiografia del torace ha rivelato un’ombra rotonda di 4 cm di diametro nel lobo inferiore del polmone destro. L’HRCT ha mostrato una formazione arrotondata,di dimensioni 4х3х2, 5 cm, strutturata in modo eterogeneo con contorni ben definiti. L’esame non è riuscito a verificare la diagnosi precisa, quindi è stata eseguita la lobectomia inferiore destra. Macroscopicamente, è stata rilevata una formazione di tipo “a nido d’ape” con contorni ben definiti e piccole cavità fino a 0,7 cm riempite con liquido marrone spesso. C’era un tessuto fibroso omogeneo denso tra le cavità. L’esame istologico ha rivelato ghiandole endometrioidi trasformate cistiche con un epitelio proliferante sulle loro pareti, nonché una formazione di papille e uno stroma citogenico fibroso, insieme a un’iperplasia leiomiomatosa attorno alle strutture ghiandolari (Figura 4).
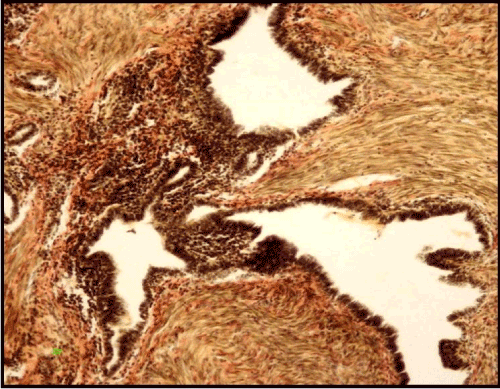
Figura. 4. Endometriosi polmonare con strutture papillari e iperplasia leiomiomatosa. Colorazione Van Gieson (X 160).
Esempio 2: Paziente A., 42 anni. La diagnosi clinica era il pneumotorace spontaneo destro. Il primo giorno del ciclo mestruale è apparso il dolore nella metà destra del torace. Era accompagnato da una tosse secca e una leggera dispnea. La radiografia del torace ha rivelato un pneumotorace destro con un’atelettasia del 50% e uno spostamento del mediastino a sinistra. Al momento del ricovero in ospedale è stata eseguita una toracoscopia diagnostica sul lato destro con un drenaggio della cavità pleurica. Il centro tendineo del diaframma mostrava perforazioni e impianti endometriali (Figura 5). L’HRCT del torace non ha rivelato cambiamenti nel tessuto polmonare. Sono state eseguite la videotoracoscopia destra, la resezione del centro del tendine del diaframma e la pleurectomia costale subtotale. Macroscopicamente, sono state rilevate alcune perforazioni nel centro del tendine e noduli brunastri con contorni ben definiti fino a 0,5 cm. Si trovavano sulla superficie del diaframma pleurico senza penetrare attraverso di esso. L’esame istologico ha mostrato alcune lesioni endometriod cistiche sullo sfondo fibroso.
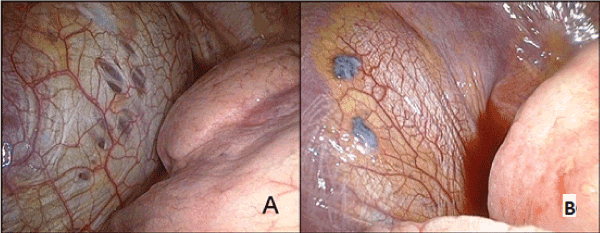
Figura. 5. Lesioni del diaframma rivelate durante il funzionamento. A-perforazioni nel centro del tendine del diaframma; B-impianti endometrioidi.
In questo caso, così come in tutti gli altri, l’insorgenza e la scomparsa dei sintomi clinici e radiologici coincidevano con l’inizio e la fine del ciclo mestruale. Tuttavia, questo fatto è sfuggito ai physisiani.
Discussione
Come chiara prova delle parole pronunciate una volta dal noto oncomorfologo russo Golovin , l’endometriosi extragenitale conferma che ogni tessuto è un’unità stabile storicamente formata che possiede determinate proprietà e potenze morfogenetiche, che non scompaiono completamente anche in caso di interrelazioni anormali tra un organismo e un tumore. Questo approccio è estremamente importante per comprendere la PE come processo patologico toto coelo.
Nella maggior parte delle nostre osservazioni, l’endometriosi ha colpito il diaframma ed è stata accompagnata dal pneumotorace con un corrispondente complesso di sintomi, mentre l’eterotopia polmonare si è verificata più raramente essendo asintomatica o fingendo alcune patologie chirurgiche e di altro tipo.
Vale la pena ricordare che la lesione della metà sinistra del torace è stata diagnosticata solo in un caso (vale a dire. nella cupola sinistra del diaframma e del polmone sinistro), che conferma il fatto che TES è la patologia del lato destro. Suggeriamo che la ragione di questa selettività sia il fatto che la cupola destra del diaframma insieme al fegato, sebbene non rigidamente legata, funziona durante la respirazione come un pistone fornendo un “effetto di aspirazione”. Presumibilmente, questo è anche il motivo per cui è esattamente lo spazio sotto la cupola del diaframma destro dove una certa quantità di sangue mestruale può arrivare dal bacino. Il riassorbimento del sangue viene effettuato con la partecipazione attiva dell’apparato linfatico del peritoneo . I frammenti endometriali raggiungono lo spazio subpleurico attraverso i vasi linfatici che perforano il diaframma e rimangono fissi nella maggior parte dei casi. La successiva necrosi e lisi dell’endometrio possono portare a difetti di perforazione. Ipoteticamente è possibile che in rari casi piccoli frammenti di endometrio raggiungano la vena cava superiore attraverso i vasi linfatici del mediastino e quindi penetrino nel parenchima polmonare formando nodi o cisti.
L’ipodiagnostica clinica e morfologica del TES è condizionata non solo dalla sua rarità, ma dalla mancanza dell’analisi complessa completa e dalla correlazione dei dati anamnestici, clinici e istologici.
Data la crescente incidenza dell’endometriosi, quella polmonare tra le altre, sembra essenziale includere questa malattia nella gamma di diagnostica differenziale, in particolare dove sono coinvolte donne in età fertile con la patologia polmonare destra non chiara e la storia ginecologica compromessa. In questi casi, è consigliabile reclutare ginecologi in modo da escludere l’adenomiosi e l’endometriosi pelvica. Nel caso delle oscure malattie polmonari ricorrenti è imperativo eseguire la risonanza magnetica dei piccoli organi pelvici.
I nostri dati consentono di determinare alcune caratteristiche importanti e affidabili del TES come segue: la localizzazione prevalentemente destra della malattia, l’età relativamente giovane dei pazienti, la recidiva ciclica dell’emottisi e il disagio o il dolore al petto, il pneumotorace destro ricorrente, la correlazione dell’insorgenza e/o regressione dei sintomi radiologici con l’inizio e/o la fine del ciclo mestruale, l’uno o l’altro dei problemi ginecologici (vale a dire. infertilità, dolore pelvico, algomenorrea) e interventi chirurgici sugli organi pelvici nell’anamnesi.
La chirurgia diagnostica richiede un uso estensivo dell’intero materiale operatorio con campioni di ritaglio per l’esame istologico di tutte le aree polmonari interessate, poiché le caratteristiche microscopiche dell’endometriosi in diverse parti del polmone, anche vicine, possono variare notevolmente. Dal punto di vista diagnostico, la caratteristica distintiva morfologica essenziale del PE è una combinazione dei segni di stabilità, progressione o regressione all’interno dello stesso o nei campioni adiacenti del tessuto polmonare. Per rendere più affidabile la diagnosi finale del TES, è necessario l’uso dei metodi istologici e immuno-istochimici completi. La diagnosi precisa dell’endometriosi è di grande importanza pratica perché è un prerequisito per una selezione del trattamento adeguato.
- Tsvelev YV, Abashin VG, et al. (2007) Endometriosi: viste moderne sull’eziologia, la terminologia e la classificazione. Vestnik Rus Accademia Medica militare 4: 42-47 .
- Olive DL, Schwartz LB (1993) Endometriosi. N Engl J Med 328: 1759-1769.
- Ozhiganova IN (2009) Endometriosi e malattia endometrioide (standard di lavoro dell’esame postmortem). SPb. .
- Harada M, Osuga Y, Izumi G, Takamura M, Takemura Y, et al. (2011) Dienogest, una nuova strategia conservativa per l’endometriosi extragenitale: uno studio pilota. Gynecol Endocrinol 27: 717-720.
- Bergqvist A (1993) Diversi tipi di endometriosi extragenitale: una recensione. Gynecol Endocrinol 7: 207-221.
- Joseph J, Sahn SA (1996) Sindrome da endometriosi toracica: nuove osservazioni da un’analisi di 110 casi. Am J Med 100: 164-170.
- Alifano M, Trisolini R, Cancellieri A, Regnard JF (2006) Endometriosi toracica: conoscenze attuali. Ann Thorac Surg 81: 761-769.
- Flieder DB, Moran CA, Travis WD, Koss MN, Mark EJ (1998) Endometriosi pleuro-polmonare e deciduosi ectopica polmonare: uno studio clinico-patologico e immuno-istochimico di 10 casi con enfasi sulle insidie diagnostiche. Hum Pathol 29: 1495-1503.
- Channabasavaiah AD e Joseph JV (2010) Endometriosi toracica: rivisitare l’associazione tra presentazione clinica e patologia toracica basata su risultati toracoscopici in 11 pazienti. Medone. Baltimora 89: 183-188.
- Legras A, Mansuet-Lupo A, Rousset-Jablonski C, Bobbio A, Magdeleinat P, et al. (2014) Pneumotorace in donne in età fertile: una classificazione di aggiornamento basata su risultati clinici e patologici. Cassa 145: 354-360.11.
- Hobbs JE e Bortnick AR. (1940) Endometriosi del polmone; uno studio sperimentale e clinico. Am J Obstet Gynecol 40: 832-843.
- Pichurov AA, OrzheshkovskiÄ OV, Dvorakovskaia IV, Romanova LA, Ivanishchak BE, et al. (2014) . Vestn Khir Im I I Grek 173: 26-29.
- Sampson JA (1927) Endometriosi peritoneale dovuta alla disseminazione mestruale del tessuto endometriale nella cavità peritoneale. Sono J Obstet. Gynecol 14: 422-469.
- Adamyan LV, Kulakov VI e Andreeva EN (2006). Endometriosi. M., Medizina. .
- Agarwal N. e Subramanian AA (2010) Endometriosi. Morfologia, presentazioni cliniche e patologia molecolare. J Medici di laboratorio 10: 1-9.
- IablonskiÄ PK, Pichurov AA, OrzheshkovskiÄ OV, Petrun’kin AM, Goncharuk IV (2014) . Vestn Khir Im I I Grek 173: 89-95.
- Terada Y, Chen F, Shoji T, Itoh H, Wada H, et al. (1999) Un caso di endometriosi endobronchiale trattata con subsegmentectomia. Cassa 115: 1475-1478. 18. Inagaki H, et al. (1999) Uso riuscito di agonista dell’ormone di rilascio della gonadotropina in un paziente con endometriosi polmonare. Respirazione 66: 544-546.
- Golovin DI (1975) Atlante dei tumori umani. Leningrado, Medizina. .
- Abu-Hijleh MF, Habbal OA, Moqattash ST (1995) Il ruolo del diaframma nell’assorbimento linfatico dalla cavità peritoneale. Giovanni 186: 453-467.