Traumatisme crânien fermé
Les traumatismes crâniens fermés sont classés comme primaires ou secondaires. Une blessure primaire résulte de l’insulte anatomique et physiologique initiale, qui est généralement un traumatisme direct à la tête, quelle qu’en soit la cause. Une lésion secondaire résulte d’une hypotension, d’une hypoxie, d’une acidose, d’un œdème ou d’autres facteurs ultérieurs pouvant endommager secondairement le tissu cérébral (voir Lésions secondaires). On pense que les radicaux libres contribuent à ces insultes secondaires, en particulier pendant l’ischémie.
Lésions primaires
La lésion primaire provoque généralement des modifications structurelles, telles qu’un hématome épidural, un hématome sous-dural, une hémorragie sous-arachnoïdienne, une hémorragie intraventriculaire ou une contusion cérébrale.
Commotions cérébrales
La commotion cérébrale est définie comme un état mental altéré qui peut inclure ou non une perte de conscience résultant d’un traumatisme crânien. La commotion cérébrale est également connue sous le nom de lésion cérébrale traumatique légère (MTBI). L’échelle de notation de l’American Academy of Neurology est largement utilisée pour classer le degré de commotions cérébrales.
Tableau 1. Échelle de notation des commotions cérébrales de l’Académie américaine de neurologie (Tableau ouvert dans une nouvelle fenêtre)
|
Grade 1 |
Grade 2 |
Grade 3 |
|
Confusion transitoire |
Confusion transitoire |
|
|
Pas de perte de conscience |
Pas de perte de conscience |
Perte de conscience brève ou prolongée |
|
Les symptômes de commotion cérébrale ou le changement d’état mental disparaissent en 15 ans |
Symptômes de commotion cérébrale ou le changement d’état mental se résout en plus de 15 minutes |
Les commotions cérébrales liées au sport sont fréquentes, avec 300 000 cas signalés chaque année. Les joueurs de football et les boxeurs sont particulièrement exposés à des commotions cérébrales répétitives, conduisant à la maladie maintenant connue sous le nom de syndrome d’encéphalopathie traumatique chronique. Les commotions cérébrales répétitives peuvent entraîner des dysfonctionnements moteurs subcliniques chroniques liés à des anomalies du système inhibiteur intracortical. Le déclin cognitif parkinsonien dû à la dégénérescence strionigrale est maintenant une conséquence bien connue des commotions cérébrales répétitives; les effets cumulatifs des lésions axonales diffuses dans le mésencéphale sont dus à une vulnérabilité accrue aux forces de cisaillement dans cette région. Augmenter la force du cou d’un joueur peut être un moyen efficace de minimiser le risque de commotions cérébrales futures, comme semblent l’indiquer les études sur les mannequins Hybrid III.
Contusion cérébrale
Les contusions cérébrales sont couramment observées dans les lobes frontal et temporal. Ils peuvent accompagner une fracture du crâne, la soi-disant contusion de fracture. Le trait le plus inquiétant de ces contusions est leur tendance à se dilater. Cela se produit généralement de 24 heures à 7 à 10 jours après la blessure initiale. Pour cette raison, les contusions cérébrales sont souvent suivies d’un nouveau scanner de la tête dans les 24 heures suivant la blessure.
Les blessures par coup (contusions) sont causées par la transmission directe de l’énergie d’impact à travers le crâne dans le cerveau sous-jacent et se produisent directement sous le site de la blessure. Les blessures à contrecoup sont causées par un cisaillement en rotation et d’autres forces indirectes qui se produisent controlatéralement à la blessure primaire. La force de rotation provoque l’impact ou le balayage des cortex frontal et temporal basaux sur des aspects rigides du crâne, de l’aile sphénoïde et des crêtes pétreuses. L’élargissement retardé des contusions intraparenchymateuses traumatiques et des hématomes est la cause la plus fréquente de détérioration clinique et de décès. Cependant, la progression de la contusion est très variable, et bien que la plupart restent inchangées pendant des jours, quelques-unes s’agrandissent, certaines assez rapidement.
Dans une étude rétrospective, des facteurs pronostiques bien connus ont été trouvés pour prédire l’élargissement de la contusion. Le facteur pronostique le plus fort est la présence d’une hémorragie sous-arachnoïdienne traumatique. La taille de l’hémorragie intraparenchymateuse signifie que les grandes lésions sont probablement dans une phase active de progression au moment de la tomodensitométrie initiale. La présence simultanée d’un hématome sous-dural était également prédictive. Les caractéristiques cliniques, telles que le score initial du Coma de Glasgow (SCG; voir le calculateur de l’échelle du Coma de Glasgow) et la pression intracrânienne (PIC), n’étaient pas prédictives de la progression. Le moment idéal pour une nouvelle analyse n’est pas clair, bien que la majeure partie de la croissance semble se produire dans les premières 24 heures suivant la blessure.
Hématome épidural
L’incidence des hématomes épiduraux est de 1% de toutes les admissions de traumatismes crâniens, comme illustré dans l’image ci-dessous. Les hématomes épiduraux résultent le plus souvent (85%) d’un saignement dans l’artère méningée moyenne. Les hématomes épiduraux, cependant, peuvent survenir à des endroits autres que dans la distribution de l’artère méningée moyenne. De tels hématomes peuvent se développer à partir de saignements de vaisseaux diploïques blessés par des fractures du crâne sus-jacentes. Les hématomes épiduraux sont souvent associés à un « intervalle lucide », une période de conscience entre états d’inconscience. La période de lucence est présumée se terminer lorsque l’hématome se dilate au point que le tronc cérébral est compromis.
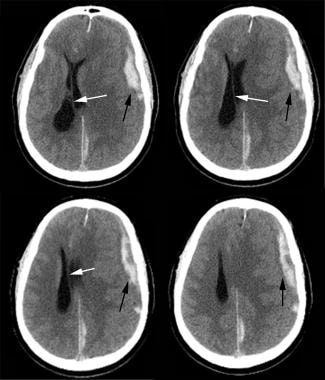 tomodensitométrie de l’hématome épidural aigu frontal gauche (flèche noire) avec décalage de la ligne médiane (flèche blanche). Notez l’hématome sous-dural falx postérieur gauche et la contusion corticale frontopariétale gauche.
tomodensitométrie de l’hématome épidural aigu frontal gauche (flèche noire) avec décalage de la ligne médiane (flèche blanche). Notez l’hématome sous-dural falx postérieur gauche et la contusion corticale frontopariétale gauche. Hématome sous-dural
La lésion intracrânienne chirurgicale la plus courante est un hématome sous-dural. Ceux-ci surviennent chez environ 20 à 40% des patients présentant des blessures graves, comme le montre l’image ci-dessous. Un vaisseau de surface ou de pontage (veineux) peut être déchiré car le parenchyme cérébral se déplace lors d’un mouvement violent de la tête. Le saignement qui en résulte provoque la formation d’un hématome dans l’espace potentiel entre le dural et l’arachnoïde. Un intervalle lucide est moins susceptible de se développer dans ce type de blessure que dans les hématomes épiduraux. Les hématomes sous-duraux peuvent également résulter d’une rupture artérielle; ces hématomes ont une localisation particulière dans la région temporopariétale et diffèrent par leur forme de ceux causés par la rupture de la veine pontante, qui se rompent généralement dans la région parasagittale frontopariétale. L’épaisseur de l’hématome et le décalage de la ligne médiane du cerveau sont souvent analysés; lorsque le décalage de la ligne médiane dépasse l’épaisseur de l’hématome (facteur de déplacement positif), un pronostic plus mauvais a été trouvé.
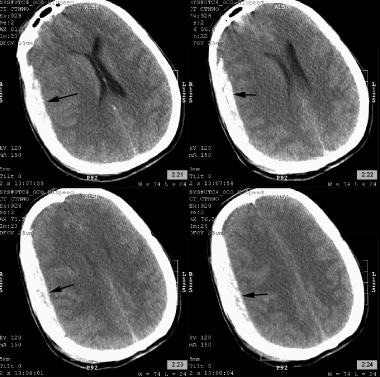 tomodensitométrie d’hématome sous-dural aigu frontopariétal gauche (flèche noire). Notez la quantité modérée de décalage de la ligne médiane.
tomodensitométrie d’hématome sous-dural aigu frontopariétal gauche (flèche noire). Notez la quantité modérée de décalage de la ligne médiane. Hémorragie intraventriculaire
Une hémorragie intraventriculaire est une autre lésion intracérébrale qui accompagne souvent d’autres hémorragies intracrâniennes, comme illustré dans l’image ci-dessous. Le sang intraventriculaire est un indicateur de traumatisme crânien plus grave. Le sang intraventriculaire prédispose également le patient à l’hydrocéphalie post-traumatique et à l’hypertension intracrânienne, ce qui peut justifier la mise en place d’un cathéter intraventriculaire (si un drainage émergent est nécessaire) ou d’un shunt ventriculopéritonéal pour l’hydrocéphalie chronique.
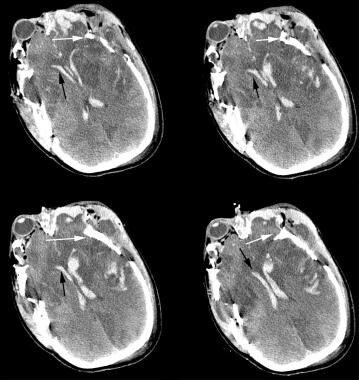 tomodensitométrie d’hémorragies intraventriculaires aiguës bilatérales (flèche noire). Notez les fractures du crâne broyées qui impliquent des os frontaux, temporaux et pariétaux bilatéraux (flèche blanche). Notez les changements ischémiques dans les deux lobes frontaux, les hémorragies sous-arachnoïdiennes dans la fissure intrahémisphérique et le lobe frontal gauche, et les hémorragies intraparenchymateuses multiples dans les deux pôles frontaux.
tomodensitométrie d’hémorragies intraventriculaires aiguës bilatérales (flèche noire). Notez les fractures du crâne broyées qui impliquent des os frontaux, temporaux et pariétaux bilatéraux (flèche blanche). Notez les changements ischémiques dans les deux lobes frontaux, les hémorragies sous-arachnoïdiennes dans la fissure intrahémisphérique et le lobe frontal gauche, et les hémorragies intraparenchymateuses multiples dans les deux pôles frontaux. Lésion axonale diffuse
Malgré l’absence de lésion de masse intracrânienne ou d’antécédents d’hypoxie, certains patients restent inconscients après un TCC. Des études d’IRM cérébrale ont démontré une corrélation claire entre les lésions de substance blanche et l’altération de la conscience après une blessure. Plus la lésion de la substance blanche est profonde, plus l’altération de la conscience est profonde et persistante.
La cause habituelle d’une altération persistante de la conscience est la condition appelée lésion axonale diffuse, comme illustré dans l’image ci-dessous. Environ 30 à 40% des personnes décédées d’un TCC révèlent des signes post-mortem d’IAD et d’ischémie. Ce type de blessure résulte généralement d’une rotation traumatique de la tête, avec des forces mécaniques qui agissent sur les longs axones, entraînant une défaillance structurelle axonale. Le DAI est causé par une blessure à l’accélération et non par une blessure de contact seule. Le cerveau est relativement incompressible et ne tolère pas bien les contraintes de traction ou de cisaillement. L’application lente de la souche est mieux tolérée que la souche rapide. Le cerveau est le plus sensible à la rotation latérale et tolère le mieux les mouvements sagittaux.
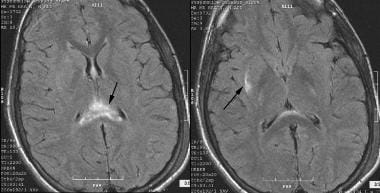 IRM du cerveau qui montre une lésion axonale diffuse (DAI) et un signal hyperintense dans le corps calleux (splénium), le septum pellucidum et la capsule externe droite.
IRM du cerveau qui montre une lésion axonale diffuse (DAI) et un signal hyperintense dans le corps calleux (splénium), le septum pellucidum et la capsule externe droite. Des études récentes suggèrent que l’amplitude de l’accélération de rotation nécessaire pour produire du DAI nécessite que la tête frappe un objet ou une surface. Ces facteurs augmentent également la probabilité que le DAI s’accompagne d’autres lésions intracrâniennes. Ces forces mécaniques disséquent physiquement ces axones en segments proximaux et distaux. Si un nombre suffisant d’axones sont impliqués, des déficits neurologiques profonds et une perte de conscience peuvent s’ensuivre.
Ces mêmes forces peuvent agir sur la circulation cérébrale, provoquant une perturbation des vaisseaux et diverses formes d’hémorragies micro–intracérébrales et d’hémorragies macro–intracérébrales, y compris les hémorragies de Duret, qui sont généralement mortelles lorsqu’elles surviennent dans le tronc cérébral. Les hémorragies de Duret du mésencéphale et des pons sont de petites hémorragies ponctuelles qui sont souvent causées par un étirement de l’artériole pendant la lésion primaire, comme illustré dans l’image ci-dessous. Ils peuvent également résulter pendant la hernie transtentoriale comme une blessure secondaire lorsque les perforateurs artériels sont comprimés ou étirés.
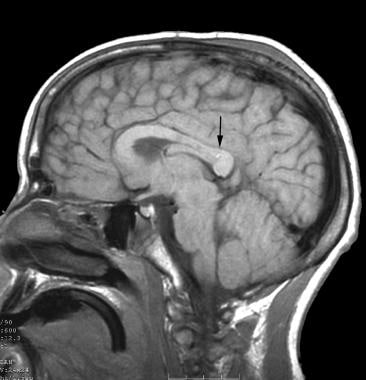 du cerveau (vue sagittale) qui montre une hémorragie de Duret dans le splénium du corps calleux.
du cerveau (vue sagittale) qui montre une hémorragie de Duret dans le splénium du corps calleux. Une étude récente indique que l’IAD et un âge plus jeune peuvent contribuer à un risque accru de développer une dysautonomie.
Blessures secondaires
Les insultes secondaires peuvent prendre plusieurs formes et peuvent être résumées comme suit:
-
Insultes intracrâniennes secondaires au cerveau
-
Hémorragie
-
Ischémie
-
Œdème
-
Pression intracrânienne élevée (PIC)
-
Vasospasme
-
Infection
-
Épilepsie
-
Hydrocéphalie
-
-
Insultes systémiques secondaires au cerveau
-
Hypoxie
-
Hypercapnie
-
Hyperglycémie
-
Hypotension
-
Hypocapnie sévère
-
Fièvre
-
Anémie
-
Hyponatrémie
-
L’objectif principal de la prise en charge des traumatismes crâniens fermés aigus est la prévention des lésions secondaires et la préservation des fonctions neurologiques qui ne sont pas endommagées par la lésion primaire.
Le vasospasme post-traumatique peut être une cause de lésion ischémique après une lésion cérébrale traumatique sévère, les contusions parenchymateuses et la fièvre étant des facteurs de risque. Les lésions mécaniques diffuses et l’activation des voies inflammatoires peuvent être des mécanismes secondaires de ce vasospasme. Les patients présentant des contusions parenchymateuses et de la fièvre peuvent bénéficier d’un dépistage supplémentaire.
Ischémie cérébrale
L’ischémie cérébrale est une perfusion insuffisante d’oxygène au cerveau à la suite d’une hypoxie ou d’une hypoperfusion. Le cerveau intact tolère mieux les faibles niveaux de PaO2 que le cerveau gravement blessé. Les tissus cérébraux traumatisés sont très sensibles à une hypoxie même modérée (90 mm Hg). Gordon et Ponten ont proposé 2 explications à ce phénomène: (1) L’alcalose respiratoire peut déplacer la courbe oxygène-hémoglobine vers la gauche, augmentant ainsi l’affinité de l’hémoglobine avec l’oxygène et diminuant la facilité de libération d’oxygène, et (2) un flux sanguin cérébral irrégulier (CBF) peut résulter d’un vasospasme focal avec perte d’autorégulation focale dans la zone du tissu cérébral lésé. Il a été démontré qu’environ un tiers des patients présentant des blessures graves à la tête présentaient des taux ischémiques de FBC.
Le CBF est normalement maintenu constant sur une plage (environ 50-150 mm Hg) de pression de perfusion cérébrale, comme illustré dans l’image ci-dessous. Ceci est rendu possible par des ajustements du tonus vasculaire connus sous le nom d’autorégulation (ligne continue). Chez les patients présentant un traumatisme cérébral, cette autorégulation peut mal fonctionner et le CBF peut devenir dépendant du CPP (lignes pointillées). L’autorégulation est absente, diminuée ou retardée chez 50% des patients présentant des blessures graves à la tête. Les valeurs de CBF les plus basses se produisent dans les 6 à 12 premières heures après la blessure. Le résultat global des patients présentant une ischémie est bien pire que celui des patients initialement non ischémiques. On pense que l’ischémie initiale cause des dommages irréversibles permanents même si la CBF est éventuellement optimisée. L’utilisation de la tomodensitométrie au xénon pour mesurer le CBF fait maintenant partie de l’arsenal pour diagnostiquer et traiter les anomalies du CBF.
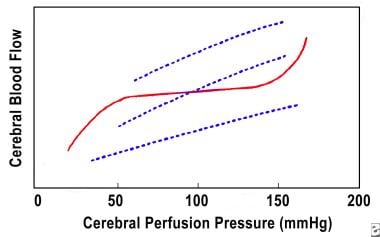 Diagramme de pression de perfusion cérébrale / débit sanguin cérébral.
Diagramme de pression de perfusion cérébrale / débit sanguin cérébral. Œdème cérébral
L’œdème cérébral est une autre forme de lésion secondaire qui peut entraîner une ICP élevée et entraîner fréquemment une mortalité accrue. L’œdème cérébral est classé en 2 principaux types: œdème vasogène et cellulaire (ou cytotoxique).
Un œdème vasogénique survient lorsqu’une brèche dans la barrière hémato-encéphalique permet à l’eau et aux solutés de se diffuser dans le cerveau. La majeure partie de ce liquide s’accumule dans la substance blanche et peut être observée sur la tomodensitométrie de la tête sous forme de substance blanche hypodense (sur les images pondérées en T1) ou sous forme de zone de signal lumineux sur l’IRM pondérée en T2. Le mécanisme de l’œdème cellulaire (cytotoxique) est moins clair. Les théories incluent l’absorption accrue de potassium extracellulaire par les cellules cérébrales blessées ou le transport de HCO3- et H + pour Cl- et Na + par le tissu cérébral blessé comme mécanisme d’insulte.
Dans une étude, l’imagerie IRM pondérée par la diffusion a été utilisée pour évaluer le coefficient de diffusion apparent (CAN) chez 44 patients atteints de TBI (GCS <8) et chez 8 volontaires sains. Des valeurs de CDA plus élevées ont été associées à un œdème vasogénique et des valeurs de CDA plus faibles ont été associées à une forme d’œdème principalement cellulaire. Des mesures régionales de l’ADC chez les patients présentant une lésion focale et diffuse ont été calculées. La conclusion finale était que le gonflement du cerveau observé chez les patients atteints de TBI semble être principalement cellulaire, comme indiqué par de faibles valeurs de CAN dans les tissus cérébraux à forte teneur en eau.