Glaucome à basse Tension: Un Oxymore en Ophtalmologie
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (Voir les affiliations de l’auteur)
Citation suggérée pour cet article: Costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. Glaucome à basse tension: Un oxymore en ophtalmologie . Précédent Dis chronique 2019; 16: 180534. DOI: http://dx.doi.org/10.5888/pcd16.180534external icône.
Le terme glaucome désigne un groupe d’affections oculaires caractérisées par une atteinte progressive du nerf optique et une perte du champ visuel (1). La neuropathie optique glaucomateuse est due à la perte progressive des cellules ganglionnaires de la rétine; une pression intraoculaire élevée (PIO) est un facteur de risque majeur. La PIO peut agir directement, par un effet mécanique, ou indirectement, en influençant l’apport sanguin (2). Les facteurs qui influencent la progression de la neuropathie optique glaucomateuse comprennent un âge plus avancé, un stade avancé de la maladie, une PIO plus élevée et des hémorragies discales (3). Chez les patients atteints de glaucome primaire à angle ouvert (POAG), la résistance accrue à l’écoulement aqueux à travers le maillage trabéculaire est le principal responsable de la PIO élevée. Cependant, malgré un contrôle adéquat de la PIO, la neuropathie optique glaucomateuse peut fréquemment continuer à progresser. Ainsi, des facteurs non liés à la PIO sont reconnus, le plus important étant une diminution de l’apport sanguin au nerf optique (4).
D’autres facteurs non liés à la PIO comprennent la toxicité du glutamate, le stress oxydatif, l’auto-immunité et la dysrégulation vasculaire (3). Le glaucome à basse tension (LTG) est défini comme une forme de glaucome qui imite étroitement le POAG, mais les taux de PIO se situent dans la plage normale et la pathogenèse probable est vasculaire.
Les questions controversées sont 1)la LTG est-elle une maladie du spectre des POAG (sur le côté gauche de la distribution de la PIO, aux niveaux les plus bas)?, 2) l’apparence du disque optique est-elle secondaire à une hypoperfusion du nerf optique due à des maladies vasculaires?, ou 3) la LTG doit-elle être incluse dans un spectre de neuropathies optiques congénitales et acquises pouvant simuler une neuropathie optique glaucomateuse?
Top
Le glaucome à Basse Tension est-il une maladie du Spectre du Glaucome Primaire à Angle Ouvert?
Lorsqu’en 1857 Albrecht von Graefe décrit une forme de glaucome se manifestant par des lésions de la tête du nerf optique et un angle de chambre antérieure ouvert, avec une PIO dans la plage de référence, la tonométrie de palpation numérique était considérée comme l’étalon-or. S’il avait utilisé un tonomètre d’impression pour mesurer la PIO, la principale lacune de la tonométrie aurait été qu’elle aurait déplacé tellement de liquide au contact de l’œil que les lectures mesurées seraient très variables et inexactes. Inversement, s’il avait utilisé la tonométrie par indentation, il n’aurait pas tenu compte de la mauvaise classification résultant de la présence d’une cornée centrale mince (1). De nombreux diagnostics de LTG concernaient des yeux avec des cornées minces et étaient basés sur de fausses valeurs basses pour la PIO, une constatation qui jette des doutes sur le diagnostic de LTG (5). De plus, l’absence de PIO élevée doit être constatée sur des mesures effectuées plus d’une fois ou pendant la journée, car la PIO présente des fluctuations diurnes et nocturnes chez les sujets sains, et encore plus chez les patients atteints de POAG ou de LTG (6). Pour les variations de la PIO, on peut distinguer 3 populations de patients atteints de LTG: les patients sans fluctuations de la PIO, les patients atteints d’acrophase diurne de la PIO (crête ou pic d’un cycle) et les patients atteints d’acrophase nocturne de la PIO (7). Les patients des 2 dernières catégories doivent être considérés comme de vrais patients atteints de POAG plutôt que comme des patients atteints de LTG, chez lesquels une neuropathie optique glaucomateuse survient malgré une PIO normale. Il est probable que des patients présentant une acrophase diurne ou nocturne ont été inscrits dans des études basées sur la théorie mécanique; la réduction de la PIO peut ralentir la progression de la perte du champ visuel uniquement chez ces patients (8). Les données de l’Étude de traitement du glaucome à basse pression ont mis en évidence le rôle de la PIO dans la pathogenèse des LTG; la progression de la perte du champ visuel a été réduite de 9,1% avec le timolol 0,5% et de 39,1% avec la brimonidine 0,2% après 2 ans de traitement (8). Cependant, dans cette étude, les valeurs de PIO ont été enregistrées exclusivement pendant la journée. Ainsi, on ignore si les patients présentant un champ visuel pire présentaient une acrophase nocturne de la PIO. D’autres études sur la LTG asymétrique ont rapporté que l’œil avec une PIO plus élevée présentait des lésions glaucomateuses plus importantes que l’œil avec une PIO plus faible, ce qui soutient le rôle de la PIO dans la pathogenèse (9). Pourtant, dans tous ces essais cliniques, la PIO n’a été mesurée que pendant les heures de bureau; ainsi, le comportement de la PIO nocturne n’a pas été enregistré. Une étude récente dans laquelle les courbes de PIO nychthémérales ont été évaluées avec un capteur télémétrique a montré une acrophase nocturne avec des pics de PIO chez les patients atteints de LTG, bien que ces pics soient à des niveaux significativement plus bas que les pics trouvés chez les patients atteints de POAG (7). Cette étude a rapporté que la PIO a atteint un pic la nuit chez 40% à 80% des patients atteints de glaucome à tension normale, et le profil chez ces patients était similaire à celui des patients atteints de POAG. Dans les courbes sur 24 heures, les patients atteints de LTG et de POAG présentaient des profils de PIO plus prononcés le soir et la nuit que le matin, avec plus de pics et une plus grande fluctuation de PIO pendant la nuit que pendant la soirée (7). D’autres facteurs peuvent corroborer l’hypothèse d’une contrainte mécanique primaire liée à la PIO dans la LTG, comme la présence de changements dans les voies d’écoulement de l’humeur aqueuse similaires à ceux qui se produisent dans la POAG (10).
Chez les patients où la LTG peut être considérée comme une maladie du spectre des POAG, des stratégies diagnostiques et thérapeutiques similaires à celles des patients atteints de glaucome hyperbare doivent être mises en œuvre, avec l’aide d’un ophtalmologiste (Figure).
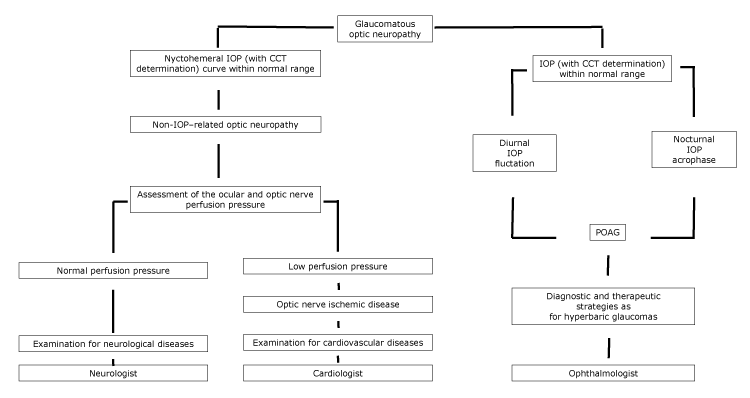
Figure.
Organigramme proposé de la neuropathie optique, avec référence spécialisée, selon les caractéristiques de la PIO nychthémérale. Abréviations: TCC, épaisseur de la cornée centrale; PIO, pression intraoculaire; POAG, glaucome primaire à angle ouvert.
Top
L’Aspect du Disque Optique Est-il Secondaire à une Hypoperfusion du Nerf Optique Due à des Maladies vasculaires?
Chez les patients présentant une LTG et des courbes normales de PIO nychthémérale, les facteurs mécaniques ne peuvent pas être responsables de la neuropathie optique; des facteurs indépendants de la pression peuvent être impliqués, les altérations vasculaires pouvant être les plus importantes (5). Une neuropathie optique de type glaucomateuse peut être observée chez les patients ayant des antécédents d’événement cardiovasculaire ou atteints d’athérosclérose chronique ou de maladies artérielles obstructives (11). Une vitesse de circulation sanguine réduite dans les artères rétrobulbaires et dans la circulation cérébrale, une pression artérielle diastolique basse et un diamètre de vaisseau rétinien central plus petit ont également été observés chez les patients atteints de LTG (5). Chez ces patients, la pathogenèse de la maladie est due à une altération de la pression de perfusion oculaire, principalement liée à une dérégulation vasculaire primaire ou à un dysfonctionnement généralisé du système nerveux endothélial ou autonome (5,11). Cependant, on ne sait pas si ces facteurs étaient la cause ou le résultat de la neuropathie optique. D’un point de vue clinique, la LTG présente une incidence plus élevée d’hémorragies discales et est plus fréquemment associée à des maladies vasculaires telles que la migraine, l’apnée obstructive du sommeil ou le syndrome de Raynaud qu’avec la PIO (5). Enfin, environ la moitié des patients atteints de LTG présentant une maladie pré-périmétrique présentent une progression des dommages malgré les valeurs normales de PIO (12). Toutes ces découvertes suggèrent le rôle important de la dysrégulation vasculaire.
Chez les patients atteints de maladies cardiovasculaires, les ventouses du disque optique peuvent avoir tendance à ne pas progresser si la cause sous-jacente de la neuropathie optique a été contrôlée. De plus, les patients atteints de LTG peuvent présenter une atrophie circumpapillaire ainsi que des micro-infarctus corticaux cérébraux, signes d’ischémie (5). Chez les patients où les maladies vasculaires induisent une hypoperfusion du nerf optique, un examen diagnostique complet des maladies cardiovasculaires doit être effectué, avec l’aide d’un cardiologue (Figure).
Top
La LTG Doit-elle Être Incluse dans un Spectre de Neuropathies Optiques Congénitales et Acquises Pouvant Simuler une Neuropathie Optique Glaucomateuse?
Lorsque les causes les plus fréquentes de ventouses du disque optique ont été exclues, la possibilité d’une neuropathie optique neurodégénérative doit être envisagée. Ces cas sont les plus frustrants, car les dommages au disque optique progressent même après que la PIO a été abaissée. De nombreuses neuropathies optiques congénitales et acquises sont incluses dans ce groupe de cas, et la différenciation entre les ventouses glaucomateuses et non glaucomateuses peut être difficile même pour les observateurs expérimentés (13). Parmi les formes congénitales de ventouses du disque optique, la mégalopapille, l’atrophie optique autosomique dominante et la neuropathie optique héréditaire de Leber pourraient produire une excavation du disque optique simulant une neuropathie optique glaucomateuse.
Les neuropathies acquises peuvent être secondaires à des causes inflammatoires, compressives, toxiques et traumatiques. La névrite optique peut entraîner une augmentation du rapport coupe-disque qui, bien qu’unilatérale, peut être confondue avec une neuropathie optique glaucomateuse. Les lésions compressives comprenant un méningiome, un adénome hypophysaire, un craniopharyngiome et un anévrisme de l’artère carotide interne peuvent entraîner une coupe asymétrique du disque optique et être attribuées à tort à la LTG. Les intoxications au méthanol et à l’éthambutol peuvent produire une forme bilatérale de ventouses du disque optique semblable à une neuropathie optique glaucomateuse, secondaire à une perte axonale. Ainsi, lorsqu’une cupule élargie asymétrique est observée, une investigation neuro-ophtalmologique plus poussée est nécessaire (13).
Enfin, parmi les conditions conduisant à la mise en forme des disques optiques, le vieillissement a un rôle principal. Harju et al ont constaté que le degré de ventouses du disque optique augmentait chez les participants à l’étude âgés en bonne santé en raison de la perte de fibres physiologiques. Leur population étudiée était appropriée et représentait un ensemble d’yeux sains sans glaucome; au cours des 11 années de suivi, aucun participant à l’étude n’a développé de modifications du champ visuel et aucune augmentation significative de la PIO n’a été enregistrée (14). Dans ce dernier cas, un examen diagnostique complet des maladies neurologiques doit être effectué, avec l’aide d’un neurologue (Figure).
Les améliorations apportées aux techniques de diagnostic facilitent la classification des ventouses du disque optique; une description des caractéristiques du disque optique combinée à l’imagerie de la couche de fibres nerveuses rétiniennes et de la topographie du disque optique permet de différencier les ventouses du disque optique glaucomateuses et non glaucomateuses. De plus, une analyse minutieuse des antécédents du patient, ainsi qu’une évaluation morphologique et fonctionnelle du nerf optique, aident à identifier les troubles.
Le terme LTG pourrait être un oxymore, un souvenir nostalgique du passé lorsqu’un diagnostic défini n’était pas possible. Utiliser le terme, c’est comme utiliser le mot « fièvre” lorsqu’il n’y a pas de température élevée ou dire festina lente (« plus de hâte, moins de vitesse”). Le terme LTG peut être trompeur ou inexact, car il fait référence à un problème mécanique de PIO, alors que les ventouses du disque optique et la perte de champ visuel dans les yeux avec une pression intraoculaire normale sont causées par d’autres facteurs. Par conséquent, en présence de ventouses de disque optique avec une PIO normale, les ophtalmologistes doivent étudier d’autres causes plausibles de lésions du nerf optique en plus de la pression intraoculaire.
Haut de la page
Remerciements
Cette étude n’a reçu aucune subvention spécifique d’un organisme de financement des secteurs public, commercial ou à but non lucratif.
Top
Informations sur l’auteur
Auteur correspondant: Luca Agnifili, MD, PhD, Clinique d’ophtalmologie, Via dei Vestini, 66100, Chieti (CH), Italie. Téléphone: +39-0871-358489. Courriel : [email protected] .
Affiliations des auteurs: 1département de Médecine et des Sciences de la Santé, Université de Molise, Campobasso, Italie. 2département de Médecine et de Sciences du vieillissement, Clinique d’ophtalmologie, Université G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14–21. Icône croisée à l’extérieur Icône PubMedexternal
- De Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; Groupe d’étude sur le traitement du glaucome à basse pression. Risk factors for visual field progression in the low-pressure glaucoma treatment study. Am J Ophthalmol 2012; 154 (4): 702-11. Icône CrossRefexternal Icône PubMedexternal
- Cartwright MJ, Anderson DR. Corrélation des dommages asymétriques avec la pression intraoculaire asymétrique dans le glaucome à tension normale (glaucome à basse tension). Arch Ophthalmol 1988; 106 (7): 898-900. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top