Low-Tension glaukooma: an Oxymoron in Oftalmology
Ciro Costagliola, MD1; Luca Agnifili, MD, PhD2; Leonardo Mastropasqua, MD2; Alfonso di Costanzo, MD1 (View author affiliations)
Suggested citation for this article: costagliola C, Agnifili L, Mastropasqua L, di Costanzo A. Low-Tension glaukooma: an Oxymoron in Oftalmology. Prev Chronic Dis 2019;16:180534. DOI: http://dx.doi.org/10.5888/pcd16.180534external icon.
termi glaukooma tarkoittaa ryhmää silmäsairauksia, joille on ominaista etenevä näköhermovaurio ja näkökentän menetys (1). Glaucomatous optinen neuropatia johtuu etenevä menetys verkkokalvon ganglion solujen; kohonnut silmänpaine (IOP) on yksi merkittävä riskitekijä. IOP voi vaikuttaa suoraan, mekaanisesti tai epäsuorasti vaikuttamalla verenkiertoon (2). Glaucomatoottisen optisen neuropatian etenemiseen vaikuttavia tekijöitä ovat vanhempi ikä, taudin pitkälle edennyt vaihe, korkeampi silmänpaine ja välilevyn verenvuoto (3). Potilailla, joilla on primaarinen avokulmaglaukooma (POAG), lisääntynyt resistenssi trabekkelikudoksen kautta tapahtuvalle vesijohtovirralle on suurin syyllinen kohonneeseen IOP: hen. IOP: n riittävästä kontrollista huolimatta glaucomatoottinen optikusneuropatia voi kuitenkin usein jatkaa etenemistään. Siten tunnistetaan tekijät, jotka eivät liity IOP: hen ja joista tärkein on näköhermon verenkierron väheneminen (4).
muita IOP: hen liittymättömiä tekijöitä ovat glutamaattitoksisuus, oksidatiivinen stressi, autoimmuunisairaus ja verisuonten säätelyhäiriö (3). Low-tension glaukooma (LTG) on määritelty muoto glaukooma, joka jäljittelee tiiviisti POAG, mutta IOP tasot ovat normaalialueella ja todennäköinen patogeneesi on verisuonten.
kiistanalaiset kysymykset ovat 1) Onko LTG tauti POAGIN spektrissä (IOP: n jakauman vasemmalla puolella, alimmilla tasoilla)?, 2) Onko optinen levy ulkonäkö toissijainen näköhermon hypoperfuusio johtuu verisuonitaudeista?, tai 3) pitäisikö LTG sisällyttää synnynnäisten ja hankittujen optisten neuropatioiden spektriin, joka voi simuloida glaucomatoottista optista neuropatiaa?
Top
onko matalajännitteinen glaukooma primaarisen Avokulmaglaukooman spektriin kuuluva sairaus?
kun Albrecht von Graefe vuonna 1857 kuvasi eräänlaisen glaukooman, joka ilmensi näköhermon pään vaurioita ja avoimen etukammion kulman, jossa IOP oli viitealueella, digitaalista tunnustelumonometriaa pidettiin kultakantaan kuuluvana. Jos hän oli käyttänyt vaikutelman tonometri mitata IOP, suurin puute tonometria olisi ollut, että se syrjäytti niin paljon nestettä joutuessaan kosketuksiin silmän, että mitatut lukemat olisi erittäin vaihteleva ja epätarkka. Sitä vastoin, jos hän olisi käyttänyt sisennystonometriaa, se ei olisi ottanut huomioon ohuen sarveiskalvon (1) esiintymisestä johtuvaa luokitteluvirhettä. Monet LTG: n diagnoosit tehtiin ohuilla sarveiskalvoilla varustetuille silmille, ja ne perustuivat vääriin alhaisiin IOP-arvoihin, mikä herättää epäilyksiä LTG: n diagnoosista (5). Kohonneen silmänpaineen puuttuminen on lisäksi todettava useammin kuin kerran tai päiväsaikaan tehdyissä mittauksissa, koska silmänpaineen vaihteluvälit näkyvät sekä päivällä että yöllä terveillä koehenkilöillä ja vielä enemmän POAG-tai LTG-potilailla (6). IOP: n vaihteluista voidaan erottaa 3 LTG-potilasryhmää: potilaat, joilla ei ollut IOP: n vaihtelua, potilaat, joilla oli vuorokautinen IOP: n akrofaasi (syklin aallonharja tai huippu) ja potilaat, joilla oli yöllinen silmänpohjan akrofaasi (7). 2 viimeisen ryhmän potilaita tulee pitää todellisina POAG-potilaina eikä LTG-potilaina, joilla esiintyy glaucomatoottista optista neuropatiaa normaalista silmänpohjasta huolimatta. On todennäköistä, että potilaita, joilla on vuorokautinen tai yöllinen akrofaasi, on otettu tutkimuksiin, jotka perustuvat mekaaniseen teoriaan; silmänpaineen pieneneminen saattaa hidastaa näkökentän menetyksen etenemistä vain näillä potilailla (8). Matalapaineisen glaukooman hoitotutkimuksen tulokset korostivat silmänpainetaudin merkitystä LTG: n patogeneesissä; näkökentän menetyksen eteneminen väheni 9, 1% timololilla 0, 5% ja 39, 1% brimonidiinilla 0, 2% 2 vuoden hoidon jälkeen (8). Tässä tutkimuksessa IOP-arvot kirjattiin kuitenkin yksinomaan päiväsaikaan. Ei siis tiedetä, oliko huonommassa näkökentässä olevilla potilailla SILMÄNPOHJAISTA AKROFAASIA. Muut epäsymmetristä LTG: tä koskevat tutkimukset raportoivat, että silmässä, jolla on korkeampi IOP, on suurempia glaucomatoottisia vaurioita kuin silmässä, jolla on alempi IOP, mikä ylläpitää IOP: n roolia patogeneesissä (9). Kaikissa näissä kliinisissä tutkimuksissa IOP mitattiin kuitenkin vain virka-aikana, joten yöllisen IOP: n käyttäytymistä ei kirjattu. Äskettäin tehdyssä tutkimuksessa, jossa nykhthemeral IOP-käyriä arvioitiin telemetrisellä anturilla, havaittiin yöllinen AKROFAASI, jossa oli SILMÄNPIIKKEJÄ LTG-potilailla, vaikka nämä piikit olivat huomattavasti alhaisempia kuin POAG-potilailla (7). Tässä tutkimuksessa raportoitiin, että silmänpainetauti oli korkeimmillaan yöllä 40-80 prosentilla normaalijännitteistä glaukoomaa sairastavista potilaista, ja näiden potilaiden malli oli samanlainen kuin POAG-potilailla. 24 tunnin käyrissä LTG: tä ja POAG: ta sairastavilla potilailla IOP oli selvemmin illalla ja yöllä kuin aamulla, ja yöllä oli enemmän huippuja ja suurempi IOP: n vaihtelu kuin illalla (7). Muut tekijät voivat vahvistaa hypoteesin ensisijaisesta IOP: hen liittyvästä mekaanisesta rasituksesta LTG: ssä, kuten se, että kammionesteen ulosvirtausreiteillä tapahtuu samanlaisia muutoksia kuin POAG: ssa (10).
potilailla, joilla LTG: tä voidaan pitää POAG: n spektriin kuuluvana sairautena, on silmälääkärin avustuksella toteutettava samanlaisia diagnostisia ja terapeuttisia strategioita kuin ylipainekaarisesta glaukoomasta kärsivillä potilailla (Kuva).
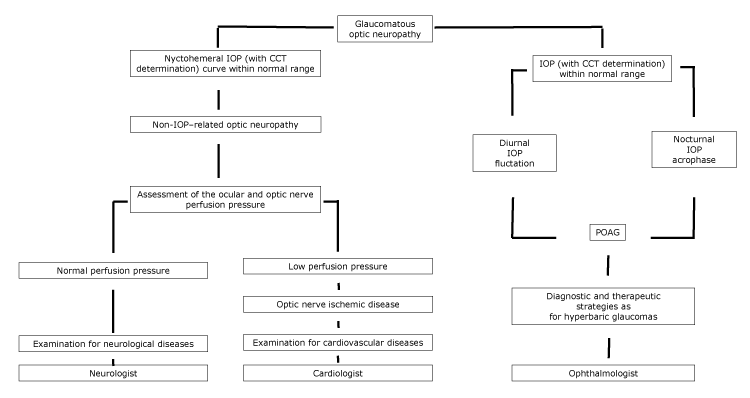
kuva.
ehdotettu optisen neuropatian vuokaavio, johon liittyy erikoislääkärin lähete, nykhthemeral IOP: n ominaisuuksien mukaan. Lyhenteet: CCT, sarveiskalvon keskipaksuus; IOP, silmänpaine; POAG, ensisijainen avokulmaglaukooma.
Top
johtuuko näköhermon hypoperfuusio verisuonisairauksista?
potilailla, joilla on LTG-ja normaalit nykhthemeraaliset IOP-käyrät, optisen neuropatian syynä eivät voi olla mekaaniset tekijät; paineesta riippumattomat tekijät voivat olla kyseessä, ja verisuonimuutokset saattavat olla tärkeimpiä (5). Glaucomatouksen kaltaista optista neuropatiaa voidaan havaita potilailla, joilla on ollut kardiovaskulaarinen tapahtuma tai krooninen ateroskleroosi tai ahtauttava valtimosairaus (11). Hidastunutta veren virtausnopeutta retrobulbaarisissa valtimoissa ja aivoverenkierrossa, alhaista diastolista verenpainetta ja pienempää verkkokalvon verisuonen halkaisijaa on havaittu myös LTG-potilailla (5). Näillä potilailla sairauden patogeneesi johtuu heikentyneestä silmän perfuusiopaineesta, joka liittyy pääasiassa primaariseen verisuonten säätelyhäiriöön tai yleiseen endoteelin tai autonomisen hermoston toimintahäiriöön (5,11). On kuitenkin epäselvää, olivatko nämä tekijät optisen neuropatian syy vai seuraus. Kliinisestä näkökulmasta LTG: ssä esiintyy enemmän välilevyvuotoja ja se liittyy useammin verisuonisairauksiin, kuten migreeniin, obstruktiiviseen uniapneaan tai Raynaudin oireyhtymään kuin IOP: ssä (5). Noin puolella perimetristä tautia sairastavista LTG-potilaista vauriot etenevät normaaleista IOP-arvoista huolimatta (12). Kaikki nämä havainnot viittaavat verisuonten säätelyhäiriön tärkeään rooliin.
sydän-ja verisuonitautipotilailla optisen levyn kuppaus ei välttämättä etene, jos optisen neuropatian perimmäinen syy on saatu hallintaan. Lisäksi LTG-potilailla voi esiintyä sirkumpapillaarisen atrofiaa sekä aivojen aivokuoren mikroinfarkteja, jotka ovat merkkejä iskemiasta (5). Potilailla, joilla verisuonisairaudet aiheuttavat näköhermon hypoperfuusion, sydän-ja verisuonitautien täydellinen diagnostinen tutkimus on suoritettava kardiologin avulla (kuva).
Top
pitäisikö LTG sisällyttää synnynnäisten ja hankittujen optisten neuropatioiden kirjoon, joka voi simuloida Glaucomatoottista optista neuropatiaa?
kun optisen levyn kuppauksen yleisemmät syyt on suljettu pois, on otettava huomioon neurodegeneratiivisen optisen neuropatian mahdollisuus. Nämä tapaukset ovat turhauttavimpia, sillä optisen levyn vauriot etenevät senkin jälkeen, kun IOP on laskettu. Monet synnynnäiset ja hankitut Optiset neuropatiat sisältyvät tähän tapauksien ryhmään, ja glaucomatousin ja nonglaucomatous kuppauksen erottaminen voi olla haastavaa jopa kokeneille tarkkailijoille (13). Niistä synnynnäinen muotoja optisen levyn kuppaus, megalopapilla, autosomaalinen hallitseva optinen atrofia, ja Leber perinnöllinen optinen neuropatia voisi tuottaa optisen levyn kaivaminen simuloimalla glaucomatous optinen neuropatia.
hankitut neuropatiat saattavat olla sekundaarisia tulehduksellisten, puristavien, toksisten ja traumaattisten syiden vuoksi. Optinen neuriitti voi tuottaa kasvua cup-to-disc suhde, joka, vaikka yksipuolinen, voidaan sekoittaa glaucomatous optinen neuropatia. Puristava leesiot kuten meningiooma, aivolisäkkeen adenoma, kraniofaryngiooma, ja sisäinen kaulavaltimon aneurysma voi johtaa epäsymmetrinen optinen levy kuppaus ja virheellisesti johtuvan LTG. Metanoli-ja etambutolimyrkytys saattaa aiheuttaa glaucomatoottisen optisen neuropatian kaltaisen molemminpuolisen optisen välilevyn kuppauksen, joka on seurausta aksonaalihäviöstä. Jos siis havaitaan epäsymmetrinen laajentunut kuppi, tarvitaan neuro-oftalmologisia lisätutkimuksia (13).
optisten levyjen kuppaukseen johtavissa olosuhteissa vanhenemisella on päärooli. Harju et al havaitsi, että optisen levyn kuppausaste nousi terveillä vanhemmilla tutkimukseen osallistuneilla fysiologisen kuituhukan vuoksi. 11 vuoden seurannan aikana yhdelläkään tutkimukseen osallistuneella ei kehittynyt näkökenttämuutoksia, eikä SILMÄNPAINETASAPAINON merkittävää nousua todettu (14). Jälkimmäisessä tapauksessa neurologisten sairauksien täydellinen diagnostinen tutkimus on suoritettava neurologin avulla (kuva).
diagnostisten tekniikoiden parannukset helpottavat optisen levyn kuppauksen luokittelua kuin ennen; optisen levyn ominaisuuksien kuvaus yhdistettynä verkkokalvon hermokuitukerroksen kuvantamiseen ja optisen levyn topografiaan mahdollistaa glaucomatoottisen ja ei-anglaukomaattisen optisen levyn kuppauksen erottelun. Lisäksi potilaan historian huolellinen analyysi yhdessä näköhermon morfologisen ja toiminnallisen arvioinnin kanssa auttaa tunnistamaan häiriöt.
termi LTG voisi olla oksymoron, nostalginen muisto menneisyydestä, jolloin määritelty diagnoosi ei ollut mahdollinen. Termin käyttäminen on kuin käyttäisi sanaa ”kuume”, kun ei ole korkeaa lämpötilaa tai sanoisi festina lente (”enemmän kiirettä, vähemmän nopeutta”). Termi LTG voi olla harhaanjohtava tai epätarkka, koska se viittaa mekaaniseen IOP-ongelmaan, kun taas optisen levyn kuppaus ja näkökentän menetys silmissä, joilla on normaali silmänpaine, johtuvat muista tekijöistä. Siksi optisen levyn kuppauksen ollessa normaalilla IOP: lla silmälääkärien tulisi tutkia silmänpaineen lisäksi muita mahdollisia näköhermovaurion syitä.
Top
kiitokset
Tämä tutkimus ei saanut erityisavustusta yhdeltäkään julkisen, kaupallisen tai yleishyödyllisen sektorin rahoittajalta.
Top
tekijätiedot
vastaava tekijä: Luca Agnifili, MD, PhD, silmätautien klinikka, Via dei Vestini, 66100, Chieti (CH), Italia. Puhelin: +39-0871-358489. Sähköposti: [email protected]
tekijän kytkökset: 1department of Medicine and Health Sciences, University of Molise, Campobasso, Italia. 2department of Medicine and Aging Science, silmätautien klinikka, University G. d’Annunzio of Chieti-Pescara, Chieti, Italy.
Top
- Coleman AL, Miglior S. Risk factors for glaucoma onset and progression. Surv Ophthalmol 2008;53(6, Suppl):S3–10. CrossRefexternal icon PubMedexternal icon
- Costagliola C, dell’Omo R, Romano MR, Rinaldi M, Zeppa L, Parmeggiani F. Pharmacotherapy of intraocular pressure: part I. Parasympathomimetic, sympathomimetic and sympatholytics. Expert Opin Pharmacother 2009;10(16):2663–77. CrossRefexternal icon PubMedexternal icon
- Weinreb RN, Aung T, Medeiros FA. The pathophysiology and treatment of glaucoma: a review. JAMA 2014;311(18):1901–11. CrossRefexternal icon PubMedexternal icon
- Cherecheanu AP, Garhofer G, Schmidl D, Werkmeister R, Schmetterer L. Ocular perfusion pressure and ocular blood flow in glaucoma. Curr Opin Pharmacol 2013;13(1):36–42. CrossRefexternal icon PubMedexternal icon
- Mastropasqua R, Fasanella V, Agnifili L, Fresina M, Di Staso S, Di Gregorio A, et al. Advance in the pathogenesis and treatment of normal-tension glaucoma. Prog Brain Res 2015;221:213–32. CrossRefexternal icon PubMedexternal icon
- Moon Y, Lee JY, Jeong DW, Kim S, Han S, Kook MS. Relationship between nocturnal intraocular pressure elevation and diurnal intraocular pressure level in normal-tension glaucoma patients. Invest Ophthalmol Vis Sci 2015;56(9):5271–9. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Mastropasqua R, Frezzotti P, Fasanella V, Motolese I, Pedrotti E, et al. Circadian intraocular pressure patterns in healthy subjects, primary open angle and normal tension glaucoma patients with a contact lens sensor. Acta Ophthalmol 2015;93(1):e14–21. CrossRefexternal icon PubMedexternal icon
- de Moraes CG, Liebmann JM, Greenfield DS, Gardiner SK, Ritch R, Krupin T; Low-pressure glaukooma Treatment Study Group. Näkökentän etenemisen riskitekijöitä matalapaineisen glaukooman hoitotutkimuksessa. Am J Oftalmol 2012;154 (4):702-11. CrossRefexternal icon PubMedexternal icon
- Cartwright MJ, Anderson DR. Correlation of asymmetric damage with asymmetric intraocular pressure glaukooma (low-tension glaukooma). Arch Ophthalmol 1988;106 (7):898-900. CrossRefexternal icon PubMedexternal icon
- Agnifili L, Carpineto P, Fasanella V, Mastropasqua R, Zappacosta A, Di Staso S, et al. Conjunctival findings in hyperbaric and low-tension glaucoma: an in vivo confocal microscopy study. Acta Ophthalmol 2012;90(2):e132–7. CrossRefexternal icon PubMedexternal icon
- Hayreh SS, Jonas JB. Appearance of the optic disk and retinal nerve fiber layer in atherosclerosis and arterial hypertension: an experimental study in rhesus monkeys. Am J Ophthalmol 2000;130(1):91–6. CrossRefexternal icon PubMedexternal icon
- Collaborative Normal-Tension Glaucoma Study Group. Comparison of glaucomatous progression between untreated patients with normal-tension glaucoma and patients with therapeutically reduced intraocular pressures. Am J Ophthalmol 1998;126(4):487–97. CrossRefexternal icon PubMedexternal icon
- Fraser CL, White AJ, Plant GT, Martin KR. Optic nerve cupping and the neuro-ophthalmologist. J Neuroophthalmol 2013;33(4):377–89. PubMedexternal icon
- Harju M, Kurvinen L, Saari J, Vesti E. Change in optic nerve head topography in healthy volunteers: an 11-year follow-up. Br J Ophthalmol 2011;95(6):818–21. CrossRefexternal icon PubMedexternal icon
Top