Anucort-HC Zäpfchen
Generischer Name: Hydrocortisonacetat
Darreichungsform: rektales Zäpfchen
Medizinisch überprüft von Drugs.com . Zuletzt aktualisiert am 1. Dezember 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Professional
- Wechselwirkungen
- Mehr
Haftungsausschluss: Dieses Medikament wurde von der FDA nicht als sicher und wirksam befunden, und diese Kennzeichnung wurde von der FDA nicht genehmigt. Weitere Informationen zu nicht zugelassenen Medikamenten finden Sie hier.
Anucort-HC Zäpfchen Beschreibung
Hydrocortisonacetat ist ein Corticosteroid, das chemisch als Pregn-4-en 3, 20-dion, 21- (acetyloxy) -11, 17-dihydroxy- (11ß) mit der folgenden Strukturformel bezeichnet wird:
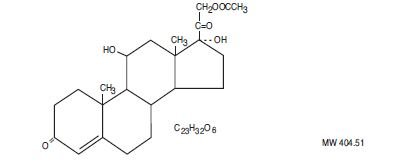
Jedes rektale Zäpfchen enthält Hydrocortisonacetat, USP 25 mg in einer speziell gemischten hydrierten Pflanzenölbasis.
Anucort-HC Suppositorium – Klinische Pharmakologie
Bei normalen Probanden werden etwa 26% des Hydrocortisonacetats absorbiert, wenn das Suppositorium auf das Rektum aufgetragen wird. Die Absorption von Hydrocortisonacetat kann über abgeriebene oder entzündete Oberflächen variieren. Topische Steroide sind in erster Linie aufgrund ihrer entzündungshemmenden, juckreizstillenden und vasokonstriktiven Wirkung wirksam.
INDIKATIONEN UND VERWENDUNG
Hydrocortisonacetat-Zäpfchen sind zur Verwendung bei entzündeten Hämorrhoiden, postbestrahlter (interstitieller) Proktitis indiziert; als Ergänzung bei der Behandlung von chronischer Colitis ulcerosa; Kryptitis; und andere entzündliche Zustände von Anorectum und Pruritus ani.
KONTRAINDIKATIONEN
Hydrocortisonacetat-Suppositorien sind bei Patienten mit Überempfindlichkeit gegen Hydrocortisonacetat oder einen der Bestandteile in der Vorgeschichte kontraindiziert.
VORSICHTSMAßNAHMEN
Verwenden Sie keine Hydrocortisonacetat-Zäpfchen, es sei denn, es wird eine angemessene proktologische Untersuchung durchgeführt.
Wenn sich eine Reizung entwickelt, sollte das Produkt abgesetzt und eine geeignete Therapie eingeleitet werden.
In Gegenwart einer Infektion sollte die Verwendung eines geeigneten antimykotischen oder antibakteriellen Mittels eingeleitet werden. Wenn ein günstiges Ansprechen nicht sofort eintritt, sollte Hydrocortisonacetat abgesetzt werden, bis die Infektion ausreichend kontrolliert wurde.
Karzinogenese: Es wurden keine Langzeitstudien an Tieren durchgeführt, um das karzinogene Potenzial von Corticosteroidsuppositorien zu bewerten.
INFORMATIONEN FÜR PATIENTEN
Bei Verwendung des Suppositoriums kann es zu Verfärbungen des Gewebes kommen. Vorsichtsmaßnahmen werden empfohlen.
SCHWANGERSCHAFTSKATEGORIE C
Bei Labortieren wurden topische Steroide mit einer Zunahme der Inzidenz von fetalen Anomalien in Verbindung gebracht, wenn trächtige Frauen eher niedrigen Dosierungen ausgesetzt waren. Es liegen keine ausreichenden und gut kontrollierten Studien bei Schwangeren vor.
Hydrocortisonacetat-Suppositorien sollten während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das Risiko für den Fötus rechtfertigt. Arzneimittel dieser Klasse sollten nicht in großem Umfang bei schwangeren Patienten, in großen Mengen oder über einen längeren Zeitraum angewendet werden.
Es ist nicht bekannt, ob dieses Arzneimittel in die Muttermilch übergeht, und da viele Arzneimittel in die Muttermilch übergehen und aufgrund des Potenzials schwerwiegender Nebenwirkungen bei stillenden Säuglingen aus Hydrocortisonacetat-Suppositorien eine Entscheidung getroffen werden sollte, ob das Stillen abgebrochen oder das Arzneimittel unter Berücksichtigung der Bedeutung des Arzneimittels für die Mutter abgesetzt werden soll.
Nebenwirkungen
Die folgenden lokalen Nebenwirkungen wurden mit Hydrocortisonacetatsuppositorien berichtet: brennen, Juckreiz, Reizung, Trockenheit, Follikulitis, Hypopigmentierung, allergische Kontaktdermatitis, Sekundärinfektion.Um VERMUTETE NEBENWIRKUNGEN zu melden, wenden Sie sich an Cosette Pharmaceuticals, Inc. bei 1-800-922-1038 oder FDA bei 1-800-FDA-1088 oder www.fda.gov/medwatch .
DROGENMISSBRAUCH UND -ABHÄNGIGKEIT
Bei Patienten, die mit Hydrocortisonacetat-Suppositorien behandelt wurden, wurde über Drogenmissbrauch und -abhängigkeit nicht berichtet.
Überdosierung
Wenn Anzeichen und Symptome einer systemischen Überdosierung auftreten, beenden Sie die Anwendung.
Anucort-HC Suppositorium Dosierung und Verabreichung
Zur rektalen Verabreichung. Lösen Sie ein Suppositorium vom Suppositorienstreifen. Zäpfchen aufrecht halten. Trennen Sie die Laschen an der oberen Öffnung und ziehen Sie sie vom spitzen Ende nach unten. Ziehen Sie weiter bis fast zur gesamten Länge des Zäpfchens nach unten. Entfernen Sie vorsichtig das Zäpfchen aus der Tasche. Vermeiden Sie eine übermäßige Handhabung des Suppositoriums, das bei Körpertemperatur schmelzen soll. Zäpfchen mit leichtem Druck in das Rektum einführen, spitzes Ende zuerst. Führen Sie bei unspezifischer Proktitis zweimal täglich morgens und abends zwei Wochen lang ein Zäpfchen in das Rektum ein. In schwereren Fällen ein Zäpfchen dreimal täglich oder zwei Zäpfchen zweimal täglich. Bei interstitieller Proktitis beträgt die empfohlene Therapiedauer je nach Ansprechen des Einzelfalls sechs bis acht Wochen oder weniger.
WIE GELIEFERT
Schachteln mit 12 Zäpfchen NDC 0713-0503-12
Schachteln mit 24 Zäpfchen NDC 0713-0503-24
Schachteln mit 100 Zäpfchen NDC 0713-0503-01
LAGERUNG UND HANDHABUNG
Bei 20-25 ° C (68 °-77 ° F) lagern. Vor Hitze schützen. Protect From Freezing.
Manufactured by:
Cosette Pharmaceuticals, Inc.
111 Coolidge Street,
South Plainfield, NJ 07080
8-0503CP1 Iss. 09/2019
PRINCIPAL DISPLAY PANEL
NDC 0713-0503-12
ANUCORT-HCTM
Hydrocortisone Acetate Suppositories
25 mg
Rx only
For Rectal Administration
12 Adult Suppositories
Cosette Pharmaceuticals, Inc.

NDC 0713-0503-24
ANUCORT-HCTM
Hydrocortisone Acetate Suppositories
25 mg
Rx only
For Rectal Administration
24 Adult Suppositories
Cosette Pharmaceuticals, Inc.

NDC 0713-0503-01
ANUCORT-HCTM
Hydrocortisone Acetate Suppositories
25 mg
Rx only
For Rectal Administration
100 Adult Suppositories
Cosette Pharmaceuticals, Inc.
HYDROCORTISONE ACETATE 25mg
Manufactured by:
Cosette Pharmaceuticals, Inc.
111 Coolidge Street,
South Plainfield,NJ 07080
| ANUCORT-HC hydrocortisone acetate suppository |
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
Labeler – Cosette Pharmaceuticals, Inc. (116918230)
Registrant – Cosette Pharmaceuticals, Inc. (116918230)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Cosette Pharmaceuticals, Inc. | 116918230 | analysis(0713-0503), label(0713-0503), manufacture(0713-0503), pack(0713-0503) | |
Mehr über Anucort-HC (hydrocortison topical)
- Nebenwirkungen
- Während der Schwangerschaft oder Stillzeit
- Dosierungsinformationen
- Wechselwirkungen mit anderen Medikamenten
- Alternativen vergleichen
- Preise & Gutscheine
- Auf Englisch
- 2 Bewertungen
- Wirkstoffklasse: topische Steroide
- FDA-Warnungen (1)
Verbraucherressourcen
- Patienteninformationen
Professionelle Ressourcen
- Verschreibungsinformationen
- Hydrocortison in Absorbase (FDA)
Andere Marken Proctozone HC, Westcort, Anusol-HC Zäpfchen, Hytone, … +18 mehr
Verwandte Behandlungsleitfäden
- Hämorrhoiden
- Analjucken
- Pruritus
Medizinischer Haftungsausschluss